Your new post is loading...

|
Scooped by
Life Sciences UPSaclay
January 3, 1:11 PM
|
Les INBS débarquent sur le site web du GIS IBiSA ! Les infrastructures nationales en biologie santé (INBS) sont au cœur de la stratégie française de recherche en science du vivant. La nouvelle page « IBiSA et les INBS » dévoile les missions du GIS pour l'organisation et la consolidation des 27 INBS inscrites sur la feuille de route du Ministère. IBiSA et les INBS. Des pages web dédiées à chacune des 27 INBS. 19 infrastructures sont déjà représentées sur le site web d'IBiSA. De nouvelles pages décrivent l'organisation de chaque INBS, précisent leurs conditions d'accès et offrent une cartographie de leurs plateformes, pour le moment limitée aux plateformes labellisées IBiSA. Les pages des 8 autres INBS seront peu à peu publiées. Explorer les INBS. Un annuaire spécial pour les plateformes des INBS. A partir des pages INBS et à l'instar de l'annuaire des plateformes IBiSA, le GIS lance un annuaire des plateformes INBS. Dans cette version encore en construction, vous retrouverez dans un premier temps les plateformes labellisées IBiSA. Étape suivante : créer des pages pour toutes les autres plateformes des INBS. Annuaire des plateformes INBS. Résultats de l'appel d’offres Plateformes IBiSA 2025. En 2025, le GIS IBiSA a reçu 77 candidatures de plateformes dans tous les domaines des sciences de la vie. Après 77 visites et 130 expertises, il a décerné 25 labels et distribué 2 210 000 € de financements à 45 plateformes technologiques en biologie, santé et agronomie. Consulter les résultats. Appel d’offres Plateformes IBiSA 2026. La prochaine édition de l'appel Plateformes IBiSA sera ouverte en janvier 2026. Les modalités de candidature seront mises à jour sur le site web. En attendant, retrouvez toute l'actualité du GIS sur les réseaux sociaux. Appel d’offres Plateformes IBiSA. A propos d’IBISA. Le GIS IBiSA coordonne la politique nationale de labellisation et de soutien aux infrastructures de biologie, santé et agronomie. Placé sous la tutelle de 8 partenaires, il est l’unique instrument de financement commun à l’ensemble des établissements de recherche en sciences du vivant. Grâce à deux appels d’offres dédiés, les plateformes et centres de ressources biologiques (CRB) peuvent candidater à la labellisation IBiSA et accéder à des financements conséquents pour des investissements jugés nécessaires à leurs missions. Le GIS conditionne son soutien à une ouverture large à la communauté scientifique. Il encourage également la création de structures de pilotage, concertation et coopération, l'animation de réseaux thématiques et les démarches qualité. Plus d'infos sur le GIS IBiSA. Vous souhaitez découvrir le potentiel de Paris-Saclay en termes de plateformes ? L’interface Plug In Labs Université Paris-Saclay recense et rend visible plus de 200 plateformes dans le domaine des sciences de la vie - des plateaux techniques, des plateformes technologiques, des infrastructures d’expérimentation, mais aussi des collections - en d’autres termes, des espaces de laboratoires dotés d’équipements, souvent uniques, ou de banques de ressources, associés à un fort potentiel humain, les opérant et les maintenant au meilleur niveau technologique. A propos de Plug In Labs Université Paris-Saclay. Plug In Labs Université Paris-Saclay ou PILUPS pour les intimes, est le portail numérique unique retenu par l’Université Paris-Saclay pour la mise en valeur et promotions des compétences, expertises et technologies des laboratoires et plateformes technologiques de son territoire. Piloté par l’Université Paris-Saclay et la SATT Paris-Saclay, financé par l’IDEX et le Fonds national de valorisation, PILUPS est accessible à tous depuis 2017, partenaires académiques comme entreprises, en particulier les PME.

|
Scooped by
Life Sciences UPSaclay
January 7, 8:31 AM
|
Le virus de la stomatite vésiculaire (VSV) est un virus oncolytique prometteur. Sa glycoprotéine G (VSV-G) est impliquée dans la reconnaissance du récepteur viral - le récepteur des lipoprotéines de basse densité (LDL-R) - et dans la fusion des membranes cellulaire et virale. VSV-G est la glycoprotéine virale la plus utilisée pour pseudotyper des vecteurs lentiviraux. Néanmoins, le récepteur du VSV est ubiquitaire et est exprimé à la surface de cellules non cibles, ce qui empêche la thérapie génique in vivo et peut aussi poser problème en oncovirothérapie. Les chercheurs de l’équipe « Rhabdovirus » de l’I2BC (CNRS/CEA/UPSaclay, Gif-sur-Yvette) avaient précédemment identifié des mutants de VSV-G qui ne se liaient plus au LDL-R mais conservaient leur activité de fusion membranaire (Nikolic et al., 2018). Dans une nouvelle étude publiée dans Molecular Therapy: Oncology, ils ont construit des glycoprotéines chimériques en fusionnant des nanobodies à l'extrémité N-terminale de VSV-G. Ces chimères étaient affectées dans leurs fonctions. Par évolution expérimentale, ils ont identifié des mutations de VSV-G qui améliorent la fonctionnalité de ces glycoprotéines chimériques, indépendamment du nanobody inséré à l'extrémité N-terminale. Ils ont ensuite généré des glycoprotéines chimériques en utilisant des nanobodies ciblant le récepteur tyrosine-protéine kinase HER2 - surexprimé à la surface des cellules cancéreuses - et introduit dans ces chimères les mutations abolissant la reconnaissance du LDL-R. Les virus (VSV ou lentivirus) pseudotypés par ces glycoprotéines infectaient spécifiquement les cellules exprimant HER2. Ces résultats établissent la preuve de concept que cette approche peut être utilisée pour conférer un nouveau tropisme à VSV-G et ouvrent la voie au développement de thérapies ciblées in vivo. -> Contact : yves.gaudin@i2bc.paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
January 7, 5:52 AM
|
IHU SEPSIS - The International Sepsis Lecture: Prof. Carolyn Calfee, January 22, 2026
📅 January 22, 2026, at 4:00 PM (Paris time) 🎤 Prof. Carolyn Calfee (University of California San Francisco, USA) 💬 The journey towards individual treatments in sepsis

|
Scooped by
Life Sciences UPSaclay
January 7, 5:31 AM
|
La Région soutient l'emploi scientifique en lien avec les besoins des entreprises en cofinançant des allocations doctorales impliquant un laboratoire académique et un partenaire socio-économique. La Région cofinance entre 100.000€ et 120.000€ maximum des allocations de recherche doctorale de 36 mois sur des projets comportant une dimension numérique sur les thématiques ci-dessous détaillées dans le texte de l'appel à projets : - Impact du changement climatique et des évènements exceptionnels (vent, canicules…) sur le bâti et l’infrastructure.
- Prévention en santé (dont santé mentale, maladies infectieuses…)
- Innovation pédagogique et usage du numérique dans l’enseignement et la formation (scolaire et supérieur)
- Modèles économiques et organisationnels des transitions énergétique, numérique, écologique…
- Impacts de la nouvelle carte des transports franciliens sur les dynamiques territoriales (grand Paris express et nouvelles lignes RER)
En savoir plus Dépôt des demandes ouvert jusqu'au 23 mars 2026 -> Contact : parisregionphd@iledefrance.fr
Objectif Financer des projets interdisciplinaires ou multi-intradisciplinaires (mettant en jeu plusieurs sous-disciplines très différentes d’une même discipline) permettant la caractérisation fonctionnelle du microenvironnement des cancers de mauvais pronostic. Il s’agit de mieux comprendre le rôle du microenvironnement tumoral dans le développement de cancers pour lesquels les options thérapeutiques sont peu efficaces et se caractérisent par un taux de survie nette standardisée 5 ans après le diagnostic inférieur à 33 %. Disciplines et domaines de recherche concernés Biochimie, mécanobiologie, biologie cellulaire, chirurgie, anatomopathologie, infectiologie, immunologie, biologie des systèmes vasculaire et lymphatique, hématologie, bio-ingénierie, analyse d’images, technologies de profilage et technologie spatiale, biologie du cancer, clinique, physique, biophysique, chimie, mathématiques. Conditions spécifiques - les projets comporteront entre 2 et 4 équipes appartenant à des disciplines ou sous-disciplines différentes ;
- les projets porteront sur des tumeurs d’emblée de mauvais pronostic, se caractérisant par un taux de survie nette standardisée 5 ans après le diagnostic inférieur à 33 % (la justification scientifique du caractère « cancer de mauvais pronostic » devra figurer dans le dossier) ;
- un même projet ne pourra pas être soumis aux appels à projets « Apports à l’oncologie des mathématiques et de l’informatique (MIC 2026) » ou « Apports de la physique, de la chimie et des sciences de l’ingénieur à l’oncologie (PCSI 2026) » ;
- une même équipe ne pourra déposer qu’un seul dossier, que ce soit en tant que coordinateur/coordinatrice de projet ou de partenaire.
Cet appel à projets est organisé par l’Inserm dans le cadre de la Stratégie décennale de lutte contre les cancers 2021 – 2030.
RAPPEL ! Assemblée Générale annuelle de la GS HeaDS - 13 janvier 2026
Nous avons le plaisir de vous convier à l’Assemblée Générale annuelle de la Graduate School Health and Drug Sciences de l’Université Paris-Saclay qui se tiendra le : Mardi 13 janvier 2026 | 12h30 à 13h30 Amphithéâtre D Bâtiment Henri Moissan 6 17 avenue des sciences 91 400 ORSAY Également en visioconférence via ce lien L’Assemblée Générale sera suivie d’un moment de convivialité autour d’un café.
Chercheurs de Paris-Saclay, candidatez au
Tech Transfer Program et bénéficiez de : - INVESTISSEMENTS : de 130k€ à 500k€
- ACCOMPAGNEMENT : de 18 à 24 mois
Dimensionnement du budget et du plan de développement, réalisé avec les experts de la SATT Paris-Saclay, lors de la période de co-construction. Déposer votre candidature Date de clôture : 6 février 2026
Via Life Sciences UPSaclay
RAPPEL ! Les Lundis de l'IPSIT - Lundi 12 janvier 2026 : « Mécanismes et applications des thérapies photodynamique et radiodynamique dans le cancer »
Lundi 12 janvier 2026 de 9h15 à 12h15 ENS Paris-Saclay - salle gradinée 1Z62- 4 avenue des sciences 91190 Gif-sur-Yvette INSCRIPTION GRATUITE MAIS OBLIGATOIRE par mail : nadine.belzic@inserm.fr (Limitation des places disponibles) Programme: - 9h15 - 9h30 Accueil des participants
- 9h30 - 10h15 : Céline FROCHOT (Directrice de recherche CNRS, LRGP UMR 7274 CNRS-Université de Lorraine, Nancy-54) : Photodynamic therapy: from fundamental research to clinical applications
- 10h15 - 10h45 Pause-café – Discussions
- 10h45 - 11h30 : Mans BROEKGAARDEN (Chargé de Recherche INSERM, direction du projet RADIOCONTROL de l'ERC Starting Grant, coordinateur du projet PANCARAS de l'ARC Pancréas, Institute for Advanced Bios-ciences, Cancer targets and Experimental therapeutics group, La Tronche) : Radiodynamic therapy with liposomal porphyrins and phthalocyanines
- 11h30 - 12h15 : Anne-Laure BULIN (Chargée de Recherche INSERM, INSERM Tenured Researcher, PI of the RADIANCE project -ERC Starting Grant-, Institute for Advanced Biosciences, Cancer targets and Experimental therapeutics group, La Tronche): Harnessing Radioluminescence for Deep-Tissue Photodynamic Therapy: Promise and Complexity

|
Scooped by
Life Sciences UPSaclay
January 6, 4:16 PM
|
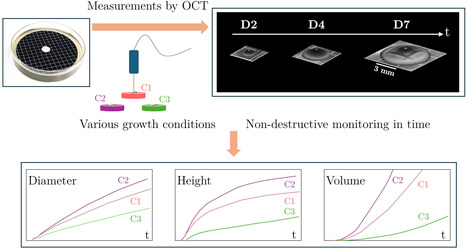
Par rapport aux cultures en suspension, la croissance microbienne dans les colonies implique une interaction complexe entre des processus biologiques et physicochimiques. Dans une étude publiée dans Biophysical Journal, les scientifiques du Laboratoire de Génie des Procédés et Matériaux (CentraleSupélec/UPSaclay, Gif-sur-Yvette), ont suivi de manière non destructive l'évolution de l'expansion des colonies immobilisées de levures (Saccharomyces cerevisiae) à l'aide de la tomographie par cohérence optique. Avec cette technique, il est possible d'obtenir des images de colonies mesurant jusqu'à 1,8 mm de hauteur et 10 mm de diamètre. Ils ont ajusté la disponibilité des nutriments en modifiant leur concentration ou l'épaisseur du gel d'agar. L’analyse des différents résultats prouve que la diffusion des nutriments, tant dans le gel d'agar qu'au sein de la colonie elle-même, est essentielle pour comprendre la dynamique de croissance des colonies. Ces résultats ont permis de valider un modèle spatio-temporel considérant le couplage entre phénomènes physiques et répartition spatiale des voies métaboliques au sein de la colonie (publication en préparation). Ce type de couplage physique et biologique a de nombreuses applications pratiques, par exemple la colonisation de cellules dans les scaffolds de reconstitution osseuse (travaux en cours). -> Contact : patrick.perre@centralesupelec.fr

|
Scooped by
Life Sciences UPSaclay
January 6, 3:56 PM
|
Les macrophages résidents du cerveau ou ‘microglies’ possèdent des fonctions importantes allant de la régulation du développement cérébral jusqu’à l'activation des réponses immunitaires innées, qui sont essentielles à la défense du système nerveux central contre diverses agressions. Ces activités sont associées à une vaste gamme d’états fonctionnels dont l’émergence est liée au contexte. Les mécanismes contrôlant ces états restent néanmoins largement méconnus. Dans une étude publiée dans Brain, Behavior, and Immunity, les scientifiques des unités UMR-S 1195 (Inserm/UPSaclay, AP-HP, Le Kremlin-Bicêtre), en collaboration avec l’UMR-S 996 (INSERM/AP-HP/UPSaclay, Orsay), l’unité de foetopathologie moléculaire de l’hôpital Antoine Beclère (APHP/UPSaclay, Clamart) et l’U1127/UMR7225 (Inserm/Cnrs/ Sorbonne Université), viennent d’identifier une petite population de microglies qui expriment le récepteur à sept domaines transmembranaires Smoothened (Smo) reconnu comme l’une des composantes clé de la voie de signalisation Hedgehog. Par des expériences gain et perte de fonction, ils montrent que l’activité intrinsèque du Smo microglial est principalement associée au déclenchement efficace des réponses immunitaires innées des microglies - plus spécifiquement de leur activité phagocytaire – face aux agents pathogènes. L’activité de Smo est également impliquée dans l’apparition des microglies amiboïdes qui surgissent transitoirement dans la substance blanche en développement et contribuent notamment à la myélinisation développementale correcte du tissu cérébral à la période périnatale. Enfin, l’activation exogène du Smo microglial se révèle capable de bloquer les cascades moléculaires pro-inflammatoires induites par les lipopolysaccharides, indépendamment de la voie de signalisation Hedgehog canonique. Tout en révélant des rôles jusqu’alors méconnus pour Smo, ces données suggèrent aussi son implication potentielle dans la réponse immunitaire innée aux infections périnatales à cytomegalovirus chez l’humain et ouvrent la porte à de futures recherches visant à découvrir une nouvelle classe d’agonistes non canoniques de Smo, susceptibles de réguler spécifiquement les états fonctionnels des microglies. -> Contact : elisabeth.traiffort@inserm.fr

|
Scooped by
Life Sciences UPSaclay
January 6, 11:41 AM
|
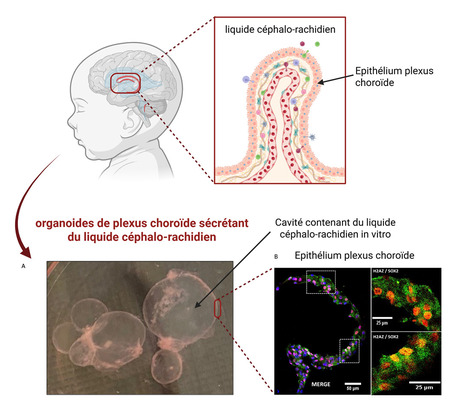
Le laboratoire d’étude de l’unité neuro-vasculaire et d’innovation thérapeutique (LENIT) (SPI/DMTS CEA/UPSaclay, Gif-sur-Yvette) dirigé par Aloïse Mabondzo a récemment publié avec des partenaires internationaux dans Fluids and Barriers of the CNS une étude sur l’impact de l’hypoxie sur l’interface plexus choroïde–liquide céphalorachidien (LCR) dans le cerveau. L’objectif était d’explorer comment l’hypoxie cérébrale dans la période autour de la naissance, condition clé de l’encéphalopathie hypoxique-ischémique perturbe cette barrière cérébrale encore peu étudiée. L’interface plexus choroïde–LCR régule la composition du liquide cérébral qui nourrit, protège et guide le développement du cerveau. En contrôlant l’apport de signaux essentiels aux neurones en formation, elle joue un rôle clé dans le bon déroulement du neurodéveloppement et participe au maintien de l’homéostasie cérébralet. Le laboratoire à mis en place un modèle organoïdes de plexus choroïdes à partir de cellules souches pluripotentes humaines capable de mimer in vitro et en trois dimensions l’épithélium du plexus choroïdes ainsi que de secréter un fluide ressemblant au LCR humain. Cet outil translationnel in vitro permet d’accéder à des cellules cérébrales humaines et au LCR pour étudier directement aux mécanismes moléculaires et les biomarqueurs responsables des altérations neurodéveloppementales observées chez les nouveau-nés victimes d’hypoxie. Les analyses après l’exposition des organoïdes de plexus choroïde à une faible teneur en oxygène suggèrent des modifications de la morphologie du plexus choroïde, des perturbations métaboliques et mitochondriales. L’analyse du protéome du LCR sécrété par ce modèle d’organoïde a permis de mettre en exergue la dérégulation de protéines potentiels biomarqueurs de l’hypoxie cérébrale, H2AZ et ITM2B. ITM2B est une protéine essentielle à la croissance des neurites et à la différenciation neuronale ; sa baisse perturbe la neurogenèse et déstabilise plusieurs voies impliquées dans la survie et le fonctionnement cellulaire. H2AZ, variante d’histone impliquée dans la régulation épigénétique, joue un rôle central dans la neurogenèse en modulant l’expression de gènes clés et en facilitant l’activation des voies dépendantes de HIF1α. Ces dérégulations pourraient ainsi contribuer aux altérations du développement neuronal en contexte d’hypoxie. Ce modèle translationnel permet de mimer de façon pertinente l’interface plexus choroïde–LCR dans le cerveau humain en développement. Dans cette étude, cet outil démontre son utilité pour étudier la physiopathologie des atteintes cérébrales et en particulier de l’hypoxie cérébrale pour découvrir de nouveaux biomarqueurs diagnostiques et thérapeutiques dans le LCR. Ce modèle préclinique translationnel permettra également de démontrer l’efficacité de candidats médicaments dans l’hypoxie cérébrale néonatale et dans d’autres affections du système nerveux central. Légende Figure : Generation of ChP organoids with fluid-filled cavities. (A) The black arrow indicates ChP epithelium and the arrowhead fluid-filled compartment. Scale bar 150 μm. (B) Immunofluorescence of ChP. Co-localization of H2AZ (red) and SOX2 (green) protein in He ChP organoids (GMB7-1 hiPSC cell line). Scale bar 50 μm and 25 μm and 40X objective, confocal microscopy, FIJI analysis -> Contact : aloise.mabondzo@cea.fr

|
Scooped by
Life Sciences UPSaclay
January 2, 9:48 AM
|
Merci à toutes et tous pour vos nombreuses contributions ! Excellente année 2026 avec toujours plus de belles découvertes dans le domaine des Sciences de la Vie !

|
Scooped by
Life Sciences UPSaclay
January 2, 5:21 PM
|
Dans une étude publiée dans Molecular Therapy, les scientifiques du laboratoire d’Isabelle Richard (UMR-S 951 Integrare Inserm/UEVE/UPSaclay, Généthon, Evry) ont évalué les effets cardiaques liés à l’administration systémique de fortes doses de vecteurs AAV utilisés en thérapie génique. Ces vecteurs, prometteurs pour le traitement des maladies monogéniques, ont montré des résultats encourageants, mais des études précliniques et des essais cliniques ont révélé que des doses élevées peuvent induire une cytotoxicité, parfois fatale. Face à des symptômes cardiaques observés chez plusieurs patients après transfert génique, l’équipe a analysé l’impact de vecteurs AAV exprimant trois transgènes associés à la dystrophie musculaire de Duchenne, à la γ-sarcoglycanopathie et à la déficience en protéine FKRP. Les chercheurs ont constaté que l’expression de ces transgènes dans le cœur pouvait provoquer une cardiotoxicité, liée à des mécanismes de surcharge protéique ou de perturbation de l’homéostasie cellulaire. En revanche, des stratégies visant à réduire ou empêcher cette expression cardiaque ont permis d’éviter ces effets indésirables. Cette innocuité a été confirmée chez des primates non humains. Ces résultats soulignent la sensibilité particulière du cœur à l’expression transgénique et l’importance de réguler finement cette expression dans toute approche de thérapie génique. Les données générées dans cet article ont servi de base pour la définition de produits de thérapie génique qui font l’objet d’essais cliniques sponsorisés par la société Atamyo Therapeutics. -> Contact : richard@genethon.fr
|

|
Scooped by
Life Sciences UPSaclay
January 8, 3:54 AM
|
L‘association Laurette Fugain joue un rôle majeur dans le financement de la recherche médicale contre les leucémies. A fin 2025, ce sont déjà plus de 11 millions d’euros qui ont été affectés à 252 projets de recherche. Cadre de l’appel d’offres : Cet appel d’offres s’adresse à tout professionnel de santé ou chercheur académique souhaitant développer un projet de recherche s’intégrant dans le cadre de la prise en charge et du parcours de soins ou du suivi des patients pédiatriques ou adultes atteints de leucémie aigüe ou chronique, de syndrome myélodysplasique ou de syndrome myéloprolifératif. - Les projets pourront prendre la forme de travaux de laboratoire, d’études épidémiologiques ou de vie réelle.
- Ils pourront porter sur l’ensemble des composantes du parcours patient, incluant le diagnostic, le pronostic et les approches thérapeutiques qu’elles soient conventionnelles (chimiothérapie, transfusion ou thérapie cellulaire par exemple) ou innovantes (immunothérapie, thérapie génétique ou ciblée par exemple).
- Une attention particulière sera portée aux projets abordant la qualité de vie des patients ou de leurs proches, ainsi que l’impact familial, professionnel et social à long terme.
- Enfin, seront également encouragées les recherches intégrant des technologies émergentes telles que l’intelligence artificielle ou les solutions digitales dédiées à l’ETP et au suivi.
Une attention spécifique, bien que non exclusive, sera portée aux projets fédérateurs (conçus et présentés par plusieurs équipes) ou multi-centriques.

|
Scooped by
Life Sciences UPSaclay
January 7, 5:56 AM
|
IHU SEPSIS - The International Sepsis Lecture: Prof. Margaret Herridge, February 24, 2026
📅 February 24, 2026, at 1:00 PM (Paris time) 🎤 Prof. Margaret Herridge (University of Toronto, Canada) 💬 Post sepsis syndrome

|
Scooped by
Life Sciences UPSaclay
January 7, 5:45 AM
|
La France, comme l’Europe, est confrontée à l’émergence sur son territoire de maladies virales animales hautement contagieuses causées par des poxvirus, touchant principalement les élevages de ruminants. Des épisodes récents, tels que la dermatose nodulaire contagieuse bovine, ont révélé la vulnérabilité des systèmes d’élevage et souligné l’importance de disposer rapidement de connaissances scientifiques solides et d’outils opérationnels pour anticiper, surveiller et maîtriser ces crises sanitaires, afin d’en limiter les impacts économiques et sociaux. Dans ce contexte, l’Agence nationale de la recherche (ANR), en coordination avec les ministères en charge de la recherche et de l’agriculture, lance un appel à projets Flash dédié aux poxvirus des ruminants (bovins, ovins et caprins), en complément des actions du PEPR Élevages Durables. Cet appel a pour objectif de mobiliser rapidement la communauté scientifique et ses partenaires afin de renforcer les connaissances, les dispositifs de surveillance, les outils de diagnostic et les stratégies de maîtrise de ces virus émergents en France et en Europe. Créé en 2010, l’instrument FLASH de l’ANR est un dispositif de financement exceptionnel destiné à soutenir, dans des délais très courts, des projets de recherche répondant à des situations d’urgence, à des enjeux émergents ou à des besoins immédiats de connaissances scientifiques. Il vise à mobiliser rapidement la communauté scientifique afin de produire des résultats opérationnels utiles à l’aide à la décision publique et à la gestion de crises sanitaires, environnementales, sociétales ou technologiques. Les projets attendus s’inscrivent dans une logique de préparation et d’anticipation des crises sanitaires animales et s’organisent autour de trois axes scientifiques : - l’étude de la diversité génétique, de l’évolution et de la virulence des poxvirus des ruminants
- le développement et l’amélioration des outils de diagnostic et de détection des poxvirus des ruminants ainsi que la caractérisation des vecteurs et des leviers de lutte
- la mise au point d’outils d’aide à la décision pour une gestion efficace des crises liées aux poxvirus des ruminants
L'aide maximum pouvant être allouée à un projet dans le cadre de cet appel est de 220 000 € (frais de gestion et de structure inclus). Documents Ouverture : 24/12/2025 à 08:00 CET Limite de soumission des dossiers : 05/02/2026 à 17:00 CET Contacts : Dr. Konstantin GRIGORIEV, PhD
Adjoint à la responsable de département EERB
Environnements, Ecosystèmes et Ressources Biologiques
Konstantin.GRIGORIEV@anr.fr Dr. Isabelle HIPPOLYTE, PhD
Responsable scientifique
Isabelle.HIPPOLYTE@anr.fr

|
Scooped by
Life Sciences UPSaclay
January 7, 5:23 AM
|
L’objet de ce programme est d’inciter les acteurs de la recherche académique à créer des partenariats structurés à travers la co-construction de « Laboratoires Communs » entre une PME ou une ETI et un laboratoire d’organisme de recherche. Un Laboratoire Commun est défini par la signature d’un contrat définissant son fonctionnement, et notamment : - une gouvernance commune,
- une feuille de route de recherche et d’innovation,
- des moyens de travail permettant d’opérer en commun la feuille de route,
- une stratégie visant à assurer la valorisation par l’entreprise du travail partenarial.
Un dispositif simple et efficace - Examen des candidatures ouvert au fil de l’eau
- Sélection s’appuyant sur un comité de pilotage
- Financement forfaitaire du laboratoire de recherche public à hauteur de 363 k€ sur 54 mois
Le dossier de candidature - Partenariat bilatéral : un organisme de recherche et une PME, ETI et Start up
- Un engagement à signer un contrat de laboratoire commun définissant :
- Une feuille de route de recherche et d’innovation
- Un programme sur au moins 54 mois, ne se limitant pas à des objectifs définis à l’avance
- Une stratégie de valorisation et de gouvernance commune
- Une stratégie de pérennité de la collaboration au-delà du soutien ANR
Un fonctionnement en deux temps 1) Phase de montage - Durée maximale souhaitée : 6 mois définie dans la proposition
- Validation par l’ANR du contrat de laboratoire commun
2) Phase de fonctionnement - Le temps restant jusqu’à T0 + 54 mois
Documents -> Contact : labcom@agencerecherche.fr
L'équipe de Julie Soutourina labellisée par la Ligue contre le cancer
Chez les eucaryotes, la transcription et la réparation de l'ADN se déroulent dans le contexte dense de la chromatine. Des dysfonctionnements de ces processus peuvent conduire à des cancers. Mediator est un complexe coactivateur multisubunitaire essentiel et conservé, muté dans de nombreux cancers. Cependant, on ignore encore largement comment Mediator et les régulateurs de la chromatine coordonnent leurs fonctions. Les travaux récents de l'équipe de Julie Soutourina (Biologie des génomes/I2BC, CEA/CNRS/UPSaclay, Gif-sur-Yvette) publiés dans Cell Reports suggèrent l'hypothèse novatrice que Mediator agit de concert avec le complexe de remodelage de la chromatine RSC (Remodels the Structure of Chromatin) de la famille SWI/SNF, homologue à PBAF (Polybromo-associated BAF) chez l'homme, représentant les complexes les plus fréquemment mutés dans les cancers. S'appuyant sur cette publication, un nouveau projet a été soutenu par la Ligue Nationale contre le cancer. En utilisant le modèle de la levure, dans la perspective d'étendre l'étude aux cellules humaines, le projet vise à décrypter les mécanismes moléculaires impliqués dans la coopération fonctionnelle entre ces complexes corégulateurs essentiels à la régulation de la transcription, à la réparation de l'ADN et à l'organisation de la chromatine, processus importants en biologie du cancer. -> Contact : julie.soutourina@i2bc.paris-saclay.fr
Via I2BC Paris-Saclay

|
Scooped by
Life Sciences UPSaclay
January 6, 4:43 PM
|
L’Institut de recherche en santé publique (IReSP) ouvre quatre volets du programme « Autonomie, grand âge et handicap ». Le programme finance des recherches sur les politiques d’autonomie, des projets en sciences humaines et sociales sur les troubles du neurodéveloppement, la mise en place et le développement de communautés mixtes de recherche, ainsi que des soutiens destinés aux doctorants et aux parcours de 4ᵉ année. Un webinaire d’information est prévu le 9 janvier.
Pour cette édition 2026, la Biodiversité sera mise à l'honneur ! Les présentations seront en anglais (exceptée la session ateliers du jeudi après-midi) Cette journée sera ponctuée de moments plus informels, propices aux échanges et pourquoi pas à de futures collaborations ! SESSION POSTER : proposée pour les enseignants/chercheurs ; chercheurs Les doctorantes/doctorants sont invités à participer. Un prix du "poster doctorant" sera remis lors de cette journée pour un montant de 500€ !
Via Life Sciences UPSaclay

|
Scooped by
Life Sciences UPSaclay
January 6, 4:25 PM
|
La chimiothérapie à base de cisplatine constitue un traitement de référence pour de nombreux cancers épithéliaux. Toutefois, l’apparition de résistances limite fortement son efficacité clinique. Malgré l’identification de multiples mécanismes associés à cette résistance, les biomarqueurs prédictifs de la réponse au cisplatine restent rares. Des travaux antérieurs avaient montré qu’une faible expression du suppresseur de tumeur NPRL2 était associée à la résistance au cisplatine. NPRL2 forme, avec NPRL3 et DEPDC5, le complexe GATOR1, un régulateur clé en amont de mTORC1, une voie fréquemment dérégulée dans les cancers résistants aux traitements. Dans une étude publiée dans Cell Death & Disease, les scientifiques de l’UMR 9018 METSY (CNRS/UPSaclay/Gustave Roussy, Villejuif) ont comparé des cellules épithéliales bronchiques non tumorales BEAS-2B délétées pour les composants de GATOR1, modélisant une résistance intrinsèque, à des lignées de cancer du poumon non à petites cellules présentant une résistance acquise au cisplatine. Les résultats montrent que la perte de n’importe quel membre du complexe GATOR1 suffit à induire une résistance au cisplatine, tandis que leur surexpression restaure la sensibilité au traitement. Cette résistance est associée à une diminution de l’accumulation intracellulaire du cisplatine, liée à une régulation différentielle des transporteurs d’entrée et de sortie du médicament, ainsi qu’à une activation accrue de la réponse aux dommages de l’ADN et de mTORC1. L’inhibition de mTORC1 permet de rétablir la sensibilité au cisplatine. Ces travaux révèlent un nouveau rôle de GATOR1 dans la résistance aux agents anticancéreux endommageant l’ADN, ouvrant la voie à de nouvelles stratégies thérapeutiques. -> Contact : svetlana.dokudovskaya@gustaveroussy.fr

|
Scooped by
Life Sciences UPSaclay
January 6, 4:06 PM
|
Les nano-microparticules (NMPs) suscitent un intérêt en médecine ou encore dans l’industrie. Toutefois, leurs propriétés physico-chimiques soulèvent des inquiétudes pour la santé humaine. Dans une étude publiée dans Chemosphere, des scientifiques de l’UMR-S 1193 (INSERM/UPSaclay, Orsay) et de l’Institut Galien Paris-Saclay (IGPS, CNRS/UPSaclay, Orsay) ont examiné la toxicité de NMPs majeures : le dioxyde de titane (TiO₂), le polystyrène (Psty) et un biopolymère à base de chitosane (CSFe). Les chercheurs ont évalué l’impact de ces NMPs sur deux acteurs de l’homéostasie cellulaire : les microtubules et les mitochondries. Ils montrent que le CSFe provoque une faible mortalité cellulaire, contrairement au Psty et au TiO₂. Le Psty 0,2 μm est étonnamment moins toxique que le Psty 0,1 μm ou 0,5 μm. De plus, le CSFe et le Psty 0,2 μm induisent une hyperacétylation des microtubules, une réponse au stress cellulaire associée à des mécanismes de survie. Le TiO₂ endommage le réseau de microtubules sans provoquer une hyperacétylation, et modifie la distribution de la protéine CLIP-170, qui n’est plus localisée exclusivement aux extrémités en croissance des microtubules, suggérant une altération du fonctionnement des microtubules révélée par une capacité de croissance perturbée. L’analyse des mitochondries révèle que le CSFe ne perturbe pas leurs morphologies, tandis que le Psty (0,1 et 0,5 μm) et le TiO2 entraînent une fragmentation de ces organites, synonyme de stress cellulaire. Cette étude souligne l’importance de la taille et de la composition des NMPs sur la réponse cellulaire et montre que les microtubules et les mitochondries constituent des biomarqueurs pertinents de la toxicité des NMPs. -> Contact : daniel.perdiz@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
January 6, 3:43 PM
|
Dans une étude multicentrique rétrospective pré-COVID récemment publiée dans International Journal of Infectious Diseases, le Dr Benjamin Davido (hôpital Raymond Poincaré, AP-HP/UVSQ/UPSaclay, Garches) et ses collaborateurs ont comparé la morbidité et la mortalité associées aux infections à human metapneumovirus (hMPV) et aux virus parainfluenza (PIV) à celles du virus respiratoire syncytial (VRS), classiquement responsable de la bronchiolite. Menée entre 2016 et 2018 au sein du réseau Paris-Saclay, cette cohorte incluait 242 patients adultes hospitalisés avec une infection respiratoire confirmée par RT-PCR (109 VRS, 89 hMPV et 44 PIV). Les résultats montrent des taux d’hospitalisation, de recours aux soins intensifs et une mortalité à 90 jours comparables entre les trois virus, soulignant un fardeau clinique similaire chez l’adulte. L’infection à hMPV était toutefois associée à une probabilité plus élevée de stabilité clinique précoce à J5 (aOR 4,22). Par ailleurs, un taux d’éosinophiles >50/mm³ apparaissait comme un marqueur pronostique favorable, associé à une amélioration rapide et à un moindre risque d’admission en réanimation, tandis que l’éosinopénie absolue constituait un puissant prédicteur d’hospitalisation. Ces résultats, illustrés par la figure présentée, rappellent que le human metapneumovirus et les virus parainfluenza, souvent considérés comme secondaires derrière le VRS, doivent être pleinement intégrés aux stratégies de surveillance et de prévention des infections respiratoires chez l’adulte compte-tenu de leur impact individuel. -> Contact : benjamin.davido@aphp.fr

|
Scooped by
Life Sciences UPSaclay
January 6, 11:31 AM
|
Portrait Jeune Chercheuse – Eleftheria Ntagia, chercheuse en technologies électrochimiques microbiennes
Eleftheria Ntagia is an environmental engineer specializing in environmental electrochemistry and microbial electrochemical technologies. She joined the PROSE unit (Procédés Biotechnologiques au Service de l'Environnement, INRAE/UPSaclay) in Antony in January 2023, focusing on microbial electrochemical systems for environmental applications. She earned her PhD in Bioscience Engineering (Environmental Sciences and Technology) from Ghent University, Belgium in 2021 under the supervision of Prof. Korneel Rabaey, Dr. Erika Fiset, and Dr. Jan Arends. Her dissertation explored the integration of electrochemical sulfide oxidation with biological carbon fixation to convert waste gases into valuable products. This work provided fundamental insights into autotrophic CO₂-reducing metabolism under sulfide stress, as well as practical knowledge on optimizing electrochemical sulfide oxidation from spent caustic streams for sulfur and caustic recovery. Continuing her focus on combining electrochemistry and microbiology, she completed a postdoctoral fellowship at the National University of Ireland, Galway, working with Prof. Piet N. L. Lens on groundwater remediation using combined biological denitrification and electrochemical disinfection. She became particularly interested in how single bioelectrochemical systems or synergistic reactor setups can enable efficient waste treatment and resource recovery while pushing the boundaries of microbial growth and metabolism. Since joining PROSE-INRAE, her research has focused on autotrophic processes within bioelectrochemical systems, with an emphasis on the sulfur and carbon cycles. She investigates bioelectrochemical CO₂ reduction and sulfide oxidation, including microbial growth under extreme conditions such as psychrotrophic and haloalkaline environments, reflecting on how these insights could redefine operational boundaries. In parallel, she explores the transformative potential of electrochemical disinfection to provide safe water solutions in remote and resource-limited regions, collaborating on projects targeting free-swimming pathogens. Eleftheria is passionate about inclusive and participatory science, mentoring early-career researchers, and opening opportunities for equal participation in scientific research. She believes that space for creativity is essential in science: “We especially need imagination in science. It is not all mathematics, nor all logic, but it is somewhat beauty and poetry.” - Maria Mitchell ->Contact : eleftheria.ntagia@inrae.fr

|
Scooped by
Life Sciences UPSaclay
January 2, 5:11 PM
|
Dans une étude publiée dans Nature Immunology, les scientifiques de l’UMR-S 1015 (Inserm/UPSaclay/Gustave Roussy, Villejuif) ont établi un atlas des cellules dendritiques (DC) humaines. Alors que les DC plasmacytoïdes (pDC) sont de mauvaises cellules présentatrices d’antigène, les DC myéloïdes (mDC), qui comprennent les DC1, DC2 et DC3, sont spécialisées dans l'activation des LT, nécessaire à une bonne réponse immunitaire anti-tumorale. Ils ont intégré les mDC provenant de 13 tissus tumoraux et juxtatumoraux issus de 40 ensembles de données de séquençage d’ARN en cellule unique pour créer le mDC-VERSE. Les sous-populations et « états » des DC dans ces tissus ont ainsi pu être caractérisés. La plupart des tumeurs étudiées contenaient une population de DC CD207+, un état commun aux DC2 et DC3, qui s'accumule dans les tumeurs de tous les carcinomes inclus dans l’étude. Leur expansion est : (1) inversement corrélée à l’expansion clonale des LT et à la fréquence des LT CD8+ résidents (TRM), et positivement corrélée aux LT CD8+ mémoire effecteurs « épuisés » dans les tumeurs ; (2) associée à une survie plus faible chez les patients ayant reçu une immunothérapie par inhibiteur de point de contrôle immunitaire (ICB). Des analyses transcriptomiques et immunohistofluorescentes spatiales en cellule unique de carcinomes humains ont démontré que les lymphocytes et la plupart des DC sont enrichis dans le stroma tumoral, tandis que les DC CD207+ sont principalement intégrées dans les nids tumoraux. Ce mDC-VERSE constitue une ressource solide à la disposition de la communauté scientifique pour étudier les DC en situation saine ou pathologique. -> Contact : charles-antoine.dutertre@inserm.fr
|



 Your new post is loading...
Your new post is loading...