Your new post is loading...

|
Scooped by
Life Sciences UPSaclay
December 7, 11:28 AM
|
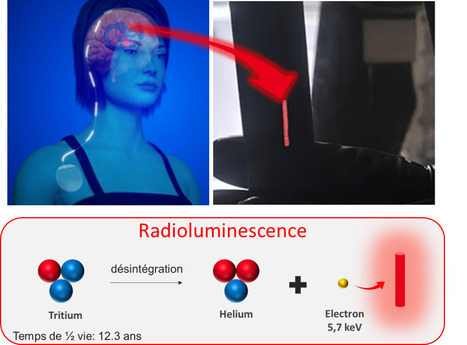
La radioluminescence ? Une R&D innovante aussi prise en charge par la plateforme de marquage isotopique du CEA (Service de Chimie Bioorganique et de Marquage (SCBM, Département Médicaments et technologies pour la Santé, Institut Joliot, CEA, Centre de Paris-Saclay). La radioluminescence, mais dans quel contexte ? La maladie de Parkinson est une pathologie neurodégénérative qui touche aujourd’hui plus de 8 millions de personnes dans le monde, avec un nombre de nouveaux cas en constante augmentation. En France, on dénombre environ 25 000 nouveaux cas chaque année. Les traitements actuellement disponibles permettent uniquement de soulager les symptômes, sans agir sur les causes profondes de la maladie. Dans ce contexte, la photobiomodulation représente un espoir prometteur pour le développement de traitements véritablement curatifs. Depuis plusieurs années, un projet de recherche innovant mené par les chercheurs de Clinatec (CEA, Grenoble) a mis en évidence l’effet de l’illumination de la substance noire sur l’évolution de la maladie dans différents modèles animaux. Actuellement, un essai clinique est en cours chez l’être humain et plusieurs patients ont déjà été implantés. Le dispositif utilisé (voir illustration, en haut à gauche, représentation schématique de l’implant actuel), se compose d’une batterie implantée sous la clavicule, d’un boîtier optique placé dans la boîte crânienne et d’une fibre optique insérée dans les ventricules cérébraux. Bien que cette approche soit prometteuse, l’implantation de la batterie et du câble la reliant à la fibre optique est invasive et donc lésionnelle pour le patient. Ainsi, le développement d’un implant autonome capable d’émettre de la lumière rouge, apparaît hautement souhaitable Et quel lien avec la plateforme de marquage isotopique ? C’est dans cette perspective qu’un projet financé par le CEA a été récemment conduit, réunissant les expertises complémentaires des chercheurs et ingénieurs de trois laboratoires du CEA de Grenoble (Clinatec, LITEN et LETI) et du laboratoire de marquage isotopique de l’Institut JOLIOT (CEA Centre de Paris-Saclay) et plus particulièrement sa plateforme de marquage isotopique. Ce projet a permis de démontrer qu’il était possible d’exploiter la radioluminescence pour concevoir de tels dispositifs (voir illustration, partie basse, principe de la radioluminescence). Les résultats obtenus ont montré que différents types de luminophores, dispersés dans des aérogels de silice ou de cellulose, peuvent être excités par les électrons issus de la désintégration du tritium (isotope radioactif de l’hydrogène, émetteur beta-moins), ouvrant ainsi la voie à la conception de nouveaux implants répondant aux exigences de compacité, d’autonomie et de puissance optique (voir illustration, en haut à droite, photographie d’un capillaire radioluminescent conçu sur la plateforme). De plus, toujours dans le cadre de ce projet, un dispositif expérimental unique a été développé au sein de la plateforme de marquage isotopique. Ce banc de mesure permet de mesurer en temps réel l’intensité lumineuse émise par un objet radioluminescent placé dans une atmosphère contrôlée. Ces travaux préliminaires très prometteurs qui ont fait l’objet d’un dépôt de brevet (FR 2113125) et d’une publication récente (Muñoz Velasco et al, 2025), seront approfondis dans le cadre du projet ANR Radiolight, dont les objectifs sont 1) d’optimiser les performances de ces implants tout en réduisant la quantité de tritium utilisée ; 2) d’étudier les effets du vieillissement sur ces matériaux ; 3) de développer de nouveaux concepts visant à générer des matériaux radioluminescents purement organique. -> Contact : Grégory Pieters (gregory. pieters@cea.fr) Plug In Labs Université Paris-Saclay : cliquer ICI MTS / Plateforme de marquage isotopique. Cette plateforme possède une expertise (unique sur Paris-Saclay) en synthèse de composés marqués avec des isotopes stables (2H / deutérium et 13C / carbone-13) et par des isotopes radioactifs de type bêta (3H / tritium, 14C / carbone-14 et 125I / iode-125). Forte de son expertise dans la préparation (synthèse, contrôle de qualité) et formulation de molécules marquées, elle assure régulièrement des prestations et collaborations, académiques comme industrielles, dans le domaine du (radio)marquage moléculaire. Elle offre également à la demande, son expertise et environnement unique de travail (laboratoires « chauds », équipements dédiés) pour l’analyse et la caractérisation d’échantillons radioactifs : mesure de puretés chimique et radiochimique par HPLC, détermination d'enrichissements isotopiques et d'activités spécifiques par SM, analyse et détermination structurale par RMN liquide comme solide, mesure d’activités radioactives par comptage à scintillation. Enfin, la plateforme propose des solutions pour le traitement de déchets liquides radioactifs, en particulier ceux contenant du carbone-14 et du tritium. A propos de l’Institut des sciences du vivant Frédéric Joliot : L’Institut des sciences du vivant Frédéric Joliot (CEA-Joliot) étudie les mécanismes du vivant pour, à la fois, produire des connaissances et répondre à des enjeux sociétaux au cœur de la stratégie du CEA : la santé et la médecine du futur, le numérique et la transition énergétique. Les travaux, fondamentaux ou appliqués, reposent sur des développements méthodologiques et technologiques. Les collaborateurs du CEA-Joliot sont pour moitié impliqués dans des unités mixtes de recherche (UMR), en partenariat avec le CNRS, l'INRAE, l’INRIA, l'Inserm, l’Université Paris-Saclay et l’Université de Paris. Le CEA-Joliot est implanté principalement sur le centre CEA-Paris-Saclay. Des équipes travaillent également à Orsay, Marcoule, Caen, Nice et Bordeaux.

|
Scooped by
Life Sciences UPSaclay
December 9, 5:04 PM
|
La mitose est un processus cellulaire fondamental, dont la défaillance a des conséquences dramatiques sur la stabilité de notre génome, pouvant conduire au cancer. Chez les mammifères, l’enveloppe nucléaire (EN), subit des modifications morphologiques importantes pendant la mitose, afin de faciliter la séparation des chromosomes. En particulier, la lamina, un réseau fibreux essentiel à la structure de l’EN, est complétement désassemblée au début de la phase mitotique et réassemblée à la fin de cette phase. En dehors de ces étapes de désassemblage/réassemblage de l’EN, la fonction de ces principaux composants, les lamines, dans le processus de la division chromosomique a longtemps été peu explorée. Dans une revue publiée dans Communications Biology, les chercheurs du laboratoire Réparation et Vieillissement de l’UMR Stabilité Génétique, Cellules souches et Radiations - SGCSR (DRCM, UMR 1274 UPSaclay/INSERM/CEA-Jacob, Fontenay-aux-Roses) mettent en lumière les liens récemment identifiés entre la mitose et les lamines, qui sont importants pour une ségrégation correcte des chromosomes. Des recherches récentes révélant les rôles multiples des lamines dans la régulation mitotique sont discutées. En effet, malgré leur désassemblage, les lamines de type A et B soutiennent la progression mitotique et la formation du fuseau mitotique. Enfin, cette revue résume les liens entre les défauts mitotiques et les dérégulations des lamines, associées fréquemment au cancer et dans des pathologies génétiques rares, et discute de leurs conséquences sur la stabilité du génome. Ainsi, cette revue apporte de nouvelles perspectives sur la contribution des lamines lors de la mitose et sur l’impact de leur dérégulation pendant cette étape essentielle du cycle cellulaire dans des contextes pathologiques, et par conséquent sur l’intégrité de notre patrimoine génétique. -> Contact : gaelle.pennarun@cea.fr / pascale.bertrand@cea.fr

|
Scooped by
Life Sciences UPSaclay
December 9, 4:54 PM
|
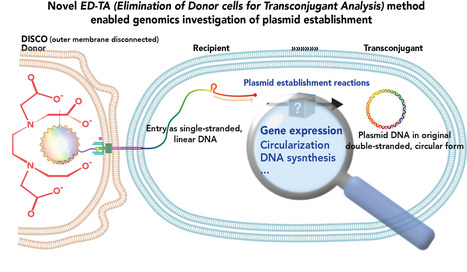
La conjugaison bactérienne est un mode principal de transfert génétique horizontal qui a des implications importantes dans les sciences de la vie, telles que l'évolution du génome bactérien, la dissémination des traits génétiques et les applications en bio-ingénierie. Notamment, La propagation de la multirésistance aux médicaments via des plasmides conjugatifs constitue l'une des plus grandes menaces pour la santé publique mondiale. Bien que la conjugaison soit étudiée depuis les années 1940, les détails moléculaires des réactions qui établissent un plasmide transféré dans la nouvelle cellule hôte restent élusifs. En outre, il existe des mécanismes de régulation spécifiques pour l'expression temporelle des gènes plasmidiques, qui sont également cruciaux pour le succès de la conjugaison, car ils permettent l'expression et le fonctionnement en temps opportun de l'arsenal codé par le plasmide contre les mécanismes de défense de l'hôte. Les études génomiques sur l'établissement des plasmides étaient auparavant limitées par la nature même de la conjugaison, qui se déroule au sein d'un mélange de populations cellulaires. Essentiellement, elles nécessitent la séparation des sous-populations avant l'extraction de l'ADN/ARN afin d'éviter la contamination par l'ADN/ARN plasmidique provenant des cellules donneuses, qui est impossible à distinguer. Dans une étude publiée dans Nucleic Acids Research, les scientifiques de l’équipe « Integrity of genome and polarity in bacteria » au sein de l’I2BC (CNRS/CEA/UPSaclay, Gif-sur-Yvette) ont décrit le développement d'une nouvelle méthode, appelée ED-TA, qui exploite un mutant donneur hypersensible au choc hypoosmotique. ED-TA permet une « élimination de la population donneuse pour l'analyse des transconjugants » d'une rapidité et d'une efficacité sans précédent. À l'aide d'un modèle cliniquement pertinent de plasmide conjugatif multirésistant, pESBL, les auteurs ont élucidé son profil de transcription dans le cadre d'une conjugaison réussie et avortée. Ils ont également montré que les promoteurs d'ADN simple brin permettent une induction robuste d'un sous-ensemble de gènes aux premiers stades de la conjugaison. La méthode ED-TA étant simple et largement applicable, des recherches supplémentaires tirant parti de cette méthode permettront de mettre en lumière d'importants mécanismes moléculaires de l'établissement du plasmide après la conjugaison. -> Contact : yoshiharu.yamaichi@i2bc.paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
December 9, 4:46 PM
|
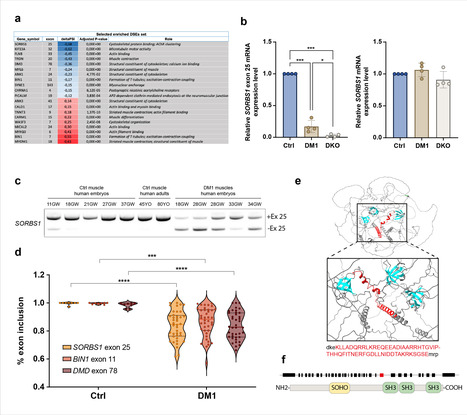
Un défaut d’épissage de SORBS1 altère la formation et la stabilité de la jonction neuromusculaire dans la dystrophie myotonique de type 1
Une étude collaborative entre des équipes de l’Institut des cellules souches pour le traitement et l’étude des maladies monogéniques – I-Stem (UMR-S 861 Inserm/AFM-Téléthon/Université Evry Paris-Saclay, Evry), de l’institut de Myologie et de l’institut Imagine (Paris) a récemment démontré les conséquences d’un défaut d’épissage alternatif dans la mise en place et la stabilité de la jonction neuromusculaire. Les auteurs démontrent que l’exon 25 du gène SORBS1, subit une exclusion anormale chez des patients atteints de la dystrophie myotonique de type 1 (DM1). L’analyse de biopsies musculaires provenant de sujets atteints de DM1 comparées à des sujets contrôles montre une réduction marquée de l’inclusion de l’exon 25. Afin d’évaluer les conséquences fonctionnelles de cette altération d’épissage, les chercheurs ont modifié in vivo chez la souris et le poisson-zèbre, et in vitro dans des cellules musculaires dérivées de cellules souches humaines (hiPSC) l’inclusion de l’exon 25. Chez la souris, l’exclusion forcée de l’exon 25 aboutit à une diminution de l’intégrité de la jonction neuromusculaire, avec une augmentation de la dénervation et une instabilité postsynaptique. Dans les cellules musculaires dérivées d’hiPSC, la formation des groupements de récepteurs à l’acétylcholine, essentielle à la transmission neuromusculaire, est également altérée. Ces résultats, publiés dans Journal of Cachexia, Sarcopenia and Muscle, suggèrent qu’un défaut d’épissage de l’exon 25 de SORBS1 constitue un mécanisme pathologique important dans la DM1, en compromettant la formation et la stabilisation de la jonction neuromusculaire. Cette étude enrichit la compréhension des conséquences fonctionnelles de l’épissage alternatif sur l’intégrité musculaire, un aspect central de la physiopathologie de la DM1. -> Contact : Mgazzola@istem.fr / Cmartinat@istem.fr

|
Scooped by
Life Sciences UPSaclay
December 9, 4:36 PM
|
Dans une étude fondamentale publiée dans Journal of the American Academy of Dermatology, les scientifiques de l’équipe Génomique Translationnelle du Cancer dirigée par Sergey Nikolaev au sein de l'UMR-S 981 (Inserm/UPSaclay/Gustave Roussy, Villejuif), de l'Université de Bordeaux (Dr Lea Dousset) et de l'Hôpital Saint-Louis (Prof Nicole Basset-Seguin), ont décrypté le carcinome basocellulaire anogénital (agBCC). Cette pathologie est ultra-rare, avec une incidence 1400 fois inférieure aux BCCs classiques, et se développe dans des zones non exposées au soleil. Menée sur une cohorte nationale de 50 patients, l’étude a révélé des caractéristiques uniques. Contrairement aux BCCs cutanés, l'agBCC présente une faible charge mutationnelle (TMB) et aucune signature liée aux rayons UV. Les analyses génomiques (séquençage du génome entier) ont démontré une dépendance quasi universelle à la voie de signalisation Sonic Hedgehog (SHH), avec l'inactivation du gène PTCH1 dans 100% des cas. L'agBCC présente également une fréquence de mutations du gène TP53 significativement réduite (16%) par rapport aux BCCs cutanés (69%). Ces résultats confirment son étiologie distincte, souvent associée au lichen scléreux ou à une radiothérapie antérieure. Cliniquement, ces tumeurs affichent un taux de récidive locale élevé (15% après excision conventionnelle), un chiffre nettement supérieur aux BCCs habituels. Ces résultats confirment la nécessité d'une vigilance accrue, et valident l'utilisation des inhibiteurs Hedgehog (HHI) comme option thérapeutique ciblée, y compris en néoadjuvant pour faciliter des chirurgies complexes. -> Contact : sergey.nikolaev@gustaveroussy.fr

|
Scooped by
Life Sciences UPSaclay
December 8, 3:43 PM
|
Portrait Jeune Chercheur – Bruno Guillotin, chercheur en biologie végétale
Bruno Guillotin est chargé de recherche CNRS au sein de l’Institut des Sciences des Plantes de Paris-Saclay - IPS2 (CNRS/INRAE/UEVE/UPSaclay, Gif-sur-Yvette) depuis février 2025. Après ses études en Biologie et Physiologie Végétale, il a effectué sa thèse de doctorat entre 2013 et 2016 au Laboratoire de recherches en Science Végétale (LRSV-Toulouse) sous la direction de Guillaume Bécard et Jean-Philippe Combier. Ses recherches portaient sur l’autorégulation de la symbiose mycorhizienne à arbuscules chez Medicago truncatula. Suite à son doctorat, il s’est orienté vers l’étude du développement des racines chez plusieurs espèces de plantes, en tant que post-doctorant dans le groupe de Kenneth Birnbaum à l’Université de New York. Là-bas, et grâce à l’obtention d’une « Human Frontiers Long-Therm Fellowship », il a développé de nombreux protocoles pour la transcriptomique en cellule unique (« single cell RNAseq ») appliqués à l’étude de l’évolution des gènes entre des espèces d’intérêt agronomique (Maïs, Sorgho, Millet), mais aussi à l’étude de la régénération cellulaire dans la racine d’Arabidopsis thaliana. En 2025 il a été recruté comme chargé de recherche CNRS, et a aussi été lauréat de la bourse ATIP-Avenir CNRS-INSERM. Aujourd'hui, à IPS2, Bruno Guillotin s'intéresse à comprendre comment les cellules de plantes communiquent entre elles via les plasmodesmes afin d’identifier quelles protéines et peptides migrent d’une cellule à l’autre et participent à la morphogenèse des organes des plantes. Ses travaux utilisent une combinaison d’approches de « single cell RNAseq », de protéomique, de génomique, et de bio-informatique. « The better we feel about these workplace relationships, the more effective we will be. » - Shawn Achor -> Contact : bruno.guillotin@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
December 2, 8:17 AM
|
Le virus de la stomatite vésiculaire (VSV) entre dans la cellule par endocytose. L’acidification de l’endosome déclenche un changement de conformation de la glycoprotéine d’enveloppe G, qui passe d’un état pré-fusion à un état post-fusion. Cela mène à la fusion des membranes virale et cellulaire, étape clef permettant la libération du génome viral dans le cytoplasme. Jusqu’à présent, la structure de VSV G complète à haute résolution restait difficile à déterminer. Dans une étude publiée dans PLOS Pathogens, des scientifiques du département de Virologie à l’I2BC (CNRS/CEA/UPSaclay, Gif-sur-Yvette), en collaboration avec l’équipe « Microscopie Electronique et Méthodes » de l’IBS à Grenoble, ont utilisé la cryo-microscopie électronique pour déterminer la structure de VSV G purifiée à partir de particules virales, sous forme libre et en complexe avec un anticorps à large spectre qui reconnaît plusieurs souches virales et conformations de VSV G. Les analyses structurales révèlent que, dans l'état post-fusion, le linker C-terminal de l'ectodomaine subit un réarrangement majeur : il se replie et s'insère dans une cavité située entre les protomères G voisins stabilisant l'assemblage trimérique post-fusion. Les structures du complexe G-anticorps identifient un épitope conservé qui reste accessible dans différents états conformationnels, expliquant la capacité de neutralisation de cet anticorps envers les vésiculovirus. Ces travaux fournissent des informations détaillées sur les mécanismes moléculaires qui permettent à VSV G de médier la fusion membranaire et illustrent comment les anticorps peuvent bloquer l'entrée. Au-delà de la virologie fondamentale, ces travaux ont des implications en recherche translationnelle, offrant des informations utiles pour la conception rationnelle de vaccins et le développement de vecteurs viraux. -> Contact : aurelie.albertini@i2bc.paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
December 3, 5:48 AM
|
La polarisation dysfonctionnelle des macrophages est fortement impliquée dans la pathogenèse de multiples affections, notamment les processus inflammatoires et la progression tumorale. Dans une étude publiée dans International Journal of Pharmaceutics, l'équipe INPACT de l'Institut Galien Paris-Saclay – IGPS (CNRS/UPSaclay, Orsay), en collaboration avec l'unité de Radiothérapie Moléculaire et Innovation Thérapeutique (UMR-S 1030 INSERM/UPSaclay/Gustave Roussy, Villejuif), s'est intéressée à la protéine P2Y2. Son inhibition est envisagée comme une stratégie permettant de reprogrammer phénotypiquement les macrophages afin de restaurer ou de renforcer leur fonctionnalité antitumorale. Pour ce faire, l'équipe a utilisé de petits ARN interférents (siRNA) capables de dégrader l’ARNm de P2Y2. Pour transporter les siRNA intacts jusqu'aux macrophages et favoriser leur internalisation cellulaire, des nanoparticules lipidiques (LNPs) ont été utilisées. L'efficacité de ces LNPs dépend de la présence à leur surface d'un conjugué phospholipide-polyéthylène glycol (Lipide-PEG). Trois types de LNPs, ne différant que par la longueur de la double chaîne lipidique de ce conjugué (C14, C16 et C18), ont été conçus. Les expériences menées sur des macrophages dérivés de la moelle osseuse de souris ont montré que toutes les formulations de LNPs étaient correctement internalisées de façon comparable. Les LNPs utilisant le DMG-PEG (C14) ont cependant démontré la plus grande efficacité, avec un niveau élevé d'inhibition et une cinétique rapide. À l'inverse, les LNPs dotées des chaînes les plus longues sont restées inefficaces plus longtemps, le siRNA restant bloqué dans des compartiments intracellulaires. Cette étude démontre donc que le choix de l'ancre lipidique du PEG est d'une importance capitale pour la performance des LNPs et leur développement dans l’objectif de moduler les fonctions des macrophages. -> Contact : elias.fattal@universite-paris-saclay.fr / francois.fay@universite-paris-saclay.fr / juliette.vergnaud@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
December 3, 8:42 AM
|
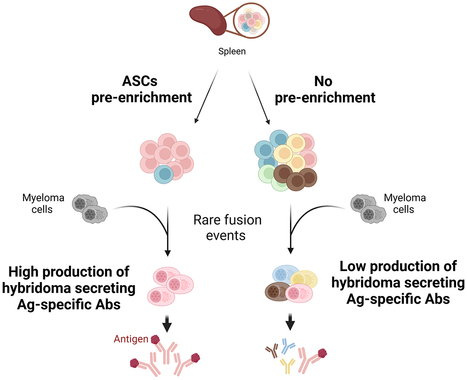
Les anticorps monoclonaux (mAbs) sont des protéines produites par les lymphocytes B qui permettent de cibler un agent pathogène particulier de manière très efficace. Il y a 50 ans, des chercheurs mettaient au point la première méthode de production en masse d'anticorps monoclonaux, appelée technologie des hybridomes : elle consiste à injecter chez l’animal l’antigène non toxique contre lequel on souhaite obtenir des anticorps afin qu’il fabrique les lymphocytes B producteurs de l’anticorps correspondant. Ces lymphocytes B sont ensuite prélevés pour être fusionnés avec des cellules cancéreuses immortalisées issues de la même lignée animale et appelées « myélomes ». De cette fusion résultent des cellules hybrides à la fois immortalisées (donc stables) et productrices d'anticorps monoclonaux : les hybridomes. Cette invention a bouleversé la recherche biomédicale en permettant le développement de nombreuses immunothérapies, tests diagnostiques et outils de laboratoire encore utilisés aujourd'hui. D'autres progrès ont depuis été réalisés afin de réduire le recours aux animaux dans les protocoles de production d'anticorps monoclonaux mais cette approche présente toujours des limites car les rendements de fusion entre les cellules productrices d'anticorps et les cellules de myélome sont faibles. Afin d'améliorer ces rendements et d’augmenter la production de nouveaux anticorps, des biologistes du Service de Pharmacologie et d'Immunoanalyse - SPI (DMTS, CEA/UPSaclay, Gif-sur-Yvette) ont travaillé sur les deux limitations principales, à savoir : le mélange aléatoire entre cellules de myélome et cellules issues de rate de souris immunisées ainsi que la faible efficacité du processus de fusion classiquement utilisé (polyéthylène-glycol). La nouvelle méthode, publiée dans mAbs, consiste d’abord à identifier les cellules productrices d'anticorps (ASCs) les plus susceptibles de s'apparier, en recourant à la cytométrie en flux (méthode d'analyse qui permet de caractériser et compter des cellules en suspension dans un flux liquidien, tel que le sang) avec un panel de cinq marqueurs de surface et des tests de sécrétion d'anticorps. Pour l’étape suivante, les biologistes ont mis au point une nouvelle stratégie qui combine le tri cellulaire et l'électrofusion (méthode de préparation des cellules hybrides pour la thérapie humaine) en ciblant les ASCs les plus prometteuses. Les chercheuses ont ainsi obtenu des hybridomes viables dans 100% des cas, contre seulement 40% pour l'électrofusion de cellules non triées. Cette optimisation de la technologie des hybridomes ouvre la voie à une nouvelle méthode de développement à haut rendement d'anticorps monoclonaux de haute affinité par fusion cellulaire. A terme, elle pourrait ainsi faciliter une utilisation plus large de cette technique fondamentale et, si elle devenait généralisée, contribuer à diminuer le nombre d’animaux nécessaires au développement et la sélection d’anticorps monoclonaux. Lire aussi l’Actu CEA-Joliot -> Contact : anne.wijkhuisen@cea.fr

|
Scooped by
Life Sciences UPSaclay
December 4, 3:51 AM
|
La transformation est un mécanisme clé de transfert horizontal de gènes, central pour l’adaptation bactérienne. Ce processus conservé au cours de l’évolution permet aux bactéries d’intégrer à leur génome du matériel génétique exogène, ce qui facilite par exemple la propagation de la résistance aux antibiotiques. Dans une étude publiée dans PNAS, des scientifiques de l’I2BC (CEA/CNRS/UPSaclay, Gif-sur-Yvette) et du DRCM/IBFJ (CEA/UPSaclay/UP Cité, Fontenay aux Roses), en collaboration avec un laboratoire du CBI (CNRS/Université de Toulouse), ont identifié un complexe protéique impliqué dans le transport de l’ADN simple brin à travers la membrane au cours de la transformation. Grâce à AlphaFold, ils ont modélisé structuralement ce complexe de trois protéines, très conservé dans le phylum des Firmicutes, en interaction avec l’ADN simple brin. Le modèle structural a permis d’identifier le cheminement possible de l’ADN à travers un canal conservé dans la protéine transmembranaire ComEC, puis le long d’un sillon formé par les deux autres protéines, ComFC et ComFA. Ce modèle a été vérifié par une stratégie expérimentale robuste dans la bactérie Streptococcus pneumoniae, en mesurant l’impact sur l’efficacité de transformation de mutations disruptives dans plusieurs interfaces protéine-protéine et protéine-ADN. Le canal transmembranaire est apparu conservé dans un modèle structural chez Helicobacter pylori, et son importance pour la transformation a également été vérifiée expérimentalement dans cette bactérie. Cette étude apporte un éclairage sur les mécanismes moléculaires de la transformation bactérienne et démontre la puissance de la prédiction de structures macromoléculaires pour proposer des hypothèses moléculaires et guider les expériences fonctionnelles. Légende Figure : (A) Machinerie et étapes de capture de l’ADN dans la transformation bactérienne chez Streptococcus pneumoniae (Sp). Les protéines étudiées sont en couleur : ComEC, protéine transmembranaire présentant un canal conservé, et le duo ComFA-ComFC, connues pour interagir l’une avec l’autre, et dont nous avons exploré l’implication dans ce processus. (B) Modèle structural par AlphaFold du complexe de trois protéines ComEC, ComFC et ComFA, en interaction avec l’ADN simple brin. -> Contact : jessica.andreani@i2bc.paris-saclay.fr / pablo.radicella@cea.fr

|
Scooped by
Life Sciences UPSaclay
December 7, 8:43 AM
|
Une étude, parue dans Journal of Clinical Oncology, a été menée en collaboration avec l’Institut Curie (Pr François-Clément Bidard, oncologue médical à l'Institut Curie, professeur à l’UFR Simone Veil-Santé, Université de Versailles Saint-Quentin-en-Yvelines/Paris-Saclay) et coordonnée par le Pr Fabrice André (UMR-S 981 INSERM/UPSaclay/Gustave Roussy, Villejuif). Elle concerne les femmes porteuses d’un cancer du sein RH positif et HER2 négatif. Elle a évalué un test pronostique reposant sur l’intelligence artificielle, développé par la start-up Spotlight Medical, dont Gustave Roussy Transfert est actionnaire. Chez les patientes porteuses de ce sous-type de la maladie classé à haut risque, le standard thérapeutique repose sur la chimiothérapie et des inhibiteurs de CDK4/6. Le test développé par Spotlight Medical suggère cependant que parmi ces patientes, certaines ne bénéficieront pas d'une intensification thérapeutique, car elles sont en réalité à faible risque de rechute. Pour parvenir à cette conclusion, les chercheurs se sont appuyés sur deux cohortes de patientes classées à haut risque. Le test de Spotlight Medical, qui analyse 10 critères histologiques ou biologiques sur des coupes numérisées de tumeurs, a permis de démontrer qu’une patiente sur cinq était en réalité à faible risque de rechute. Des résultats validés par les données en vie réelle, puisque parmi les femmes identifiées, 95,4 % n’ont pas fait de rechute après un suivi de neuf ans. Ce test pourrait, à terme, permettre de personnaliser la prise en charge de ces patientes. -> Contact : francois-clement.bidard@curie.fr / fabrice.andre@gustaveroussy.fr

|
Scooped by
Life Sciences UPSaclay
December 2, 8:07 AM
|
Portrait Jeune Chercheuse – Sophie de Carné Trécesson, Chaire de Professeur Junior en prévention des cancers
Sophie de Carné Trécesson studies the early events that drive the progression of pre-cancerous lesions toward malignancy, focusing on the interactions between cancer cells and their surrounding normal cells. Her goal is to understand how external factors – known as the exposome – contribute to tumourigenesis and identify ways to prevent cancer before it emerges. A cell biologist and junior group leader at Gustave Roussy, she leads the Inflammation and Cancer Plasticity Laboratory (UMR-S 981 Inserm/UPSaclay/Gustave Roussy, IHU‑PRISM, Villejuif). Her team investigates how environmental and metabolic factors influence the transformation of KRAS-mutated cells, which are frequently observed in lung and pancreatic cancers. After completing her PhD at the University of Angers and a first postdoctoral position in Nantes, Sophie joined the Francis Crick Institute in London, where she spent nearly ten years studying tumour plasticity and immune evasion in response to RAS signalling or cancer therapy. She returned to France in 2024 to establish her independent laboratory at Gustave Roussy and was appointed Junior Professor Chair (CPJ) in Cancer Prevention at Université Paris‑Saclay in March 2025. Her research combines patient samples, organoid models, murine systems and single-cell technologies to explore how the exposome creates a biological context that favours tumour promotion. By identifying early molecular and cellular changes involved in this transition, she aims to develop targeted prevention strategies that could reduce cancer incidence and alleviate the burden on healthcare systems. Beyond its scientific aspects, Sophie sees cancer prevention as a societal and economic priority. With rising healthcare costs and increasing patient numbers, she believes prevention is both economically and ethically necessary. Her years in the United Kingdom profoundly influenced her scientific approach and societal outlook. Sophie is deeply attached to British culture, its collaborative spirit and its commitment to inclusivity in science. She later obtained British citizenship and was selected as one of the 2025 Franco-British Young Leaders, which gives her a platform to strengthen links between science, public policy and society, and to establish prevention as an essential component of future cancer research and public health. “Improving prevention is critical to protect more lives and to preserve the sustainability of our healthcare systems.” -> Contact : sophie.de-carne@gustaveroussy.fr

|
Scooped by
Life Sciences UPSaclay
December 7, 7:00 AM
|
Chaque 1er décembre, la Journée mondiale de lutte contre le sida rappelle que, malgré les avancées majeures, le VIH reste un défi scientifique, médical et sociétal. Depuis plusieurs décennies, le CEA s’engage aux côtés de nombreux partenaires pour mieux comprendre l’infection, accélérer l’innovation thérapeutique et renforcer les stratégies de prévention. Rencontre avec Roger Le Grand, directeur d'IDMIT (CEA-Jacob, Université Paris-Saclay, Fontenay-aux-Roses) et spécialiste des maladies infectieuses, qui revient sur les différents enjeux scientifiques. Lire la suite de l’Actu CEA et voir la vidéo de l'entretien -> Contact : roger.le-grand@cea.fr
|

|
Scooped by
Life Sciences UPSaclay
December 9, 5:10 PM
|
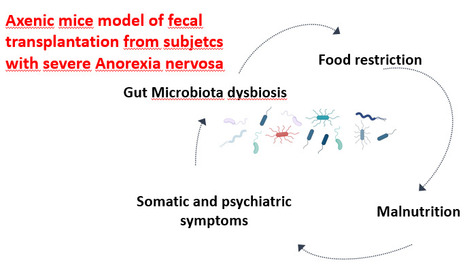
Dans une étude publiée dans Gut Microbes les scientifiques de l’Institut MICALIS (INRAE/AgroParisTech/UPSaclay, Jouy-en-Josas) ont étudié le rôle de la dysbiose du microbiote intestinal (MI) rapportée dans l'anorexie mentale (AM), dans la genèse de l’ensemble du spectre des symptômes de la maladie. Pour cela, ils ont développé un modèle murin de transplantation de microbiote fécal (TMF), en utilisant des souris BALB/c axéniques colonisées avec des échantillons fécaux de patientes atteintes d’AM bien phénotypées et de témoins sains. Les paramètres physiologiques, somatiques et comportementaux ont été recueillis de manière systématique. Il a été constaté que des symptômes clés liées à l’AM (notamment la restriction alimentaire, les symptômes anxieux, l’hyperactivité physique et des réponses inflammatoires élevées) étaient transmis à des souris axéniques après transplantation d’un microbiote issu de patientes souffrant d’AM et en situation de dénutrition comparativement à des souris transplantées avec du microbiote de donneurs sains. De plus, des atteintes d’organes associées à l’AM, telles les anomalies hépatiques, la perturbation des cycles et des follicules ovariens, ont également été reproduites. En conclusion, le transfert de microbiote provenant de patientes avec AM induit des altérations comportementales, physiologiques et d’organes rappelant la symptomatologie humaine. Ces résultats mettent en évidence un rôle majeur du microbiote intestinal dans l’expression et la progression de l’AM et ouvrent de nouvelles perspectives thérapeutiques ciblant cet écosystème. -> Contact : mouna.hanachi@aphp.fr

|
Scooped by
Life Sciences UPSaclay
December 9, 4:58 PM
|
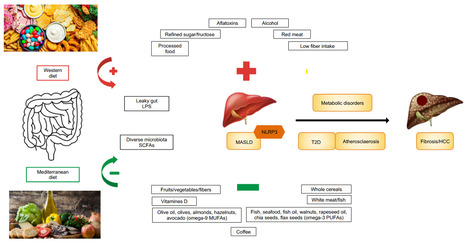
La stéatopathie métabolique (MASLD, metabolic dysfunction-associated steatotic liver disease) est désormais le principal facteur de risque de carcinome hépatocellulaire dans les pays occidentaux, en raison de l’évolution des habitudes alimentaires. Dans une revue narrative récemment publiée dans Nutrition Reviews, les équipes du service d’hépato-gastroentérologie et nutrition de l’hôpital Antoine-Béclère (AP-HP) et de l’UMR-S 996 (INSERM/AP-HP/UPSaclay, Orsay), en collaboration avec l’International Agency for Research on Cancer (IARC, Lyon), synthétisent les connaissances sur le lien entre alimentation et développement de ce cancer. L’analyse de la littérature montre que les facteurs nutritionnels associés à un risque accru de carcinome hépatocellulaire incluent : la contamination par des aflatoxines, la consommation de viandes rouges et transformées, un apport élevé en acides gras saturés, les aliments à forte charge glycémique et l’alcool, même modéré. À l’inverse, une alimentation riche en légumes, légumineuses, fruits et céréales complètes — sources de fibres, polyphénols et glucides à faible index glycémique — pourrait atténuer le microenvironnement hépatique pro-tumorigène. Sur le plan physiopathologique, la revue met en évidence le rôle central de l’inflammation chronique de bas grade (méta-inflammation), la résistance à l’insuline et les perturbations du microbiote intestinal dans la carcinogenèse hépatique. Les auteurs soulignent l’importance des interventions nutritionnelles pour promouvoir une alimentation saine, réduisant ainsi le risque de carcinome hépatocellulaire, y compris chez les patients sans fibrose hépatique avancée, actuellement exclus des stratégies de dépistage. Légende Figure : Interaction des facteurs alimentaires avec l'axe intestin–foie et la méta-inflammation. HCC, hepatocellular carcinoma ; LPS, lipopolysaccharide ; MASLD, metabolic dysfunction–associated steatotic liver disease ; MUFA, monounsaturated fatty acid ; NLRP3, NOD-like receptor pyrin domain containing 3 ; PUFA, polyunsaturated fatty acid ; SCFA, short-chain fatty acid ; T2D, type 2 diabetes. -> Contact : cosmin.voican@aphp.fr

|
Scooped by
Life Sciences UPSaclay
December 9, 4:49 PM
|
L’ingénierie d’« ordinateurs microbiens », capables d’effectuer des tâches logiques, est un pilier de la biologie de synthèse et présente de nombreuses applications potentielles industrielles et médicales. Dans un article publié dans Biotechnology Advances, les chercheurs de l’équipe Bio-RetroSynth de l’Institut Micalis (INRAE/AgroParisTech/UPSaclay, Jouy-en-Josas) retracent la genèse de ces dispositifs ainsi que leur évolution conceptuelle au cours des deux dernières décennies. Ils soulignent les limites des premiers circuits génétiques et analysent les différents paradigmes mis en œuvre afin de s’affranchir de ces contraintes. S’inspirant du reservoir computing, une approche étudiée en intelligence artificielle, ils proposent finalement de concevoir une nouvelle génération de « bio-ordinateurs » basée sur l’exploitation et l’ingénierie des circuits computationnels naturellement présents chez les micro-organismes. -> Contact : paul.ahavi@inrae.fr / jean-loup.faulon@inrae.fr

|
Scooped by
Life Sciences UPSaclay
December 9, 4:41 PM
|
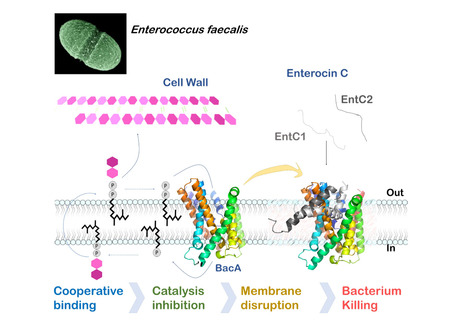
La résistance aux antibiotiques constitue un enjeu majeur de santé publique, soulignant l’urgence de développer de nouvelles stratégies thérapeutiques. Dans ce contexte, les bactériocines apparaissent comme des alternatives antibactériennes prometteuses. Dans une étude publiée dans Journal of Biological Chemistry, des scientifiques de l’I2BC (CNRS/CEA/UPSaclay, Gif-sur-Yvette) et de l’institut MICALIS (INRAE/UPSaclay, Jouy-en-Josas) ont révélé le mécanisme moléculaire d’une bactériocine à deux peptides, l’Entérocine C, doté d’une forte activité contre Enterococcus faecalis, un pathogène opportuniste majeur connu pour sa multirésistance. Ils ont démontré que l’Entérocine C exploite la protéine membranaire BacA comme récepteur à la surface de la cellule cible. BacA, largement conservée dans le monde bactérien, joue un rôle clé dans la biogenèse de la paroi grâce à son activité de recyclage du transporteur lipidique undécaprényl phosphate. En combinant des approches biochimiques, biophysiques et microbiologiques, appuyées par une modélisation structurelle AlphaFold, ils ont décrypté l’action coopérative des deux peptides de l’entérocine C. À des concentrations nanomolaires, le peptide EntC1 s’insère profondément dans la poche catalytique ouverte vers l’extérieur de BacA, inhibant son activité enzymatique et facilitant la liaison du peptide EntC2. Cet ancrage coopératif au sein du cœur hydrophobe de la membrane déclenche une perméabilisation de la membrane menant à la mort cellulaire. Ces résultats révèlent les déterminants moléculaires de ce ciblage de haute précision. Ils identifient BacA comme une cible de choix par des bactériocines et ouvrent la voie à la conception rationnelle de peptides antimicrobiens afin de développer des traitements sur mesure contre les infections résistantes aux antibiotiques. -> Contact : thierry.touze@i2bc.paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
December 9, 4:32 PM
|
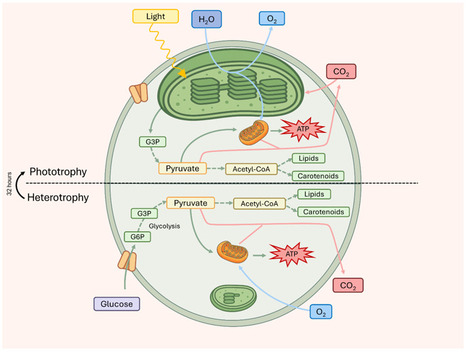
La production industrielle de microalgues est aujourd’hui à un croisement. D'un côté, la photosynthèse, produisant des cellules de très grande qualité (fort taux de protéines, teneur élevée en pigments ayant des vertus antioxydantes), mais avec une productivité encore trop limitée. De l'autre côté, la fermentation, dont les rendements sont exceptionnels, mais au prix de taux de protéines et de pigments plus faibles. Une solution existe pour réconcilier ces deux approches : la photo-induction, c’est-à-dire leur alliance séquentielle. Mais les progrès à l'échelle du procédé industriel sont ralentis par l'absence de connaissance fine des mécanismes cellulaires sous-jacents. Ainsi, la Chaire de Biotechnologie de CentraleSupélec (LGPM) a mené la première étude visant à identifier les différentes phases par lesquelles passent les microalgues lors d’une transition de la fermentation vers la photosynthèse. L’équipe a utilisé la microalgue modèle Chlorella vulgaris (microalgue verte) pour mener des expériences de transition sous différentes intensités lumineuses (de douces à extrêmes). Cinq grandes étapes (indépendantes de l’intensité lumineuse) ont pu être identifiées : activation des gènes (environ 3 heures), reprise de la photosynthèse (entre 9 et 17 heures), réactivation de la division cellulaire (à environ 24 heures), reprise de la synthèse des pigments (vers 32 heures), et retour à une croissance photosynthétique stable (au bout de 72 heures). Ces résultats, publiés dans Bioresource Technology, offrent enfin une compréhension claire des mécanismes en jeu et fourniront une base solide pour améliorer et industrialiser cette méthode de production de microalgues. -> Contact : victor.pozzobon@centralesupelec.fr
RAPPEL ! Fondation Lefoulon-Delalande - Bourses de Recherche 2026
Créées en 2001, les Bourses de Recherche de la Fondation Lefoulon-Delalande ont pour but de promouvoir les activités d’un chercheur post-doctorant travaillant à plein temps dans le domaine cardio-vasculaire au sein d’une structure de recherche française ; les stages de recherche correspondant à un premier post-doctorat au sein de la même structure, et les stages de recherche à l’étranger n’étant pas recevables.
Le sujet de recherche peut porter sur le développement, la physiologie, les pathologies, l’épidémiologie, les thérapeutiques médicales ou chirurgicales cardio-vasculaires à l’exclusion des recherches portant sur la cancérologie.
Le candidat doit être titulaire d’un doctorat en médecine, sciences, pharmacie ou vétérinaire ou d’un diplôme équivalent. Des bourses d’une durée de deux ans, d’un montant de 100 000 euros chacune toutes charges comprises (cotisations retraites, charges sociales), seront attribuées au titre de 2024. Ce montant pourra être porté à 115 000 euros selon l’ancienneté du bénéficiaire et l’appartenance institutionnelle de son laboratoire de recherche. Chaque candidature doit être parrainée par un laboratoire d’accueil qui recevra le montant de la bourse, à charge pour lui de la servir au bénéficiaire et d’établir avec lui un contrat à durée déterminée (CDD) de deux ans. - DATE LIMITE DE DÉPÔT DES DOSSIERS : 29 JANVIER 2026
DATE DE DÉCISION D’ATTRIBUTION : AVRIL 2026 - Plus d'informations

|
Scooped by
Life Sciences UPSaclay
December 2, 8:54 AM
|
Avec l'intensification du réchauffement climatique et la fréquence accrue des épisodes de chaleur extrême, le problème du stress thermique chez les cultures s'aggrave. Bien que l'on sache que les plantes réagissent au stress environnemental par une reprogrammation métabolique et une régulation épigénétique, la synergie entre ces deux mécanismes demeure un mystère scientifique majeur. Dans une étude publiée dans Nature Communications, des chercheurs de l’Institut des Sciences des Plantes de Paris-Saclay - IPS2 (CNRS/INRAE/UEVE/UPSaclay, Gif-sur-Yvette) en collaboration avec le l’Université d’Agriculture de Huazhong ont mis en évidence qu'une pyruvate kinase (PK1) peut simultanément moduler les voies métaboliques et remodeler la chromatine, conférant à la plante une tolérance à la chaleur. En fait, PK1 est elle-même induite par le stress thermique et s’accumule dans le noyau cellulaire, favorisant l’accumulation nucléaire de pyruvate et d’acétyl-CoA, la phosphorylation d’histone H3 au niveau de la thréonine en position 11 (H3T11p), mais aussi l’acétylation de l’histone H3 au niveau de la lysine en position 9 (H3K9ac). Cette dernière est due à la phosphorylation et activation de l’histone acétyltransférase GCN5 par PK1. De manière réciproque, GCN5 acétyle également PK1, renforçant son activité kinase sur les voies métaboliques et le remodelage de la chromatine. Cette régulation réciproque permet l’activation des gènes impliqués dans la tolérance au stress thermique, d’une part, et l’accumulation des métabolites antioxydants (pyruvate) et substrat pour l’acétylation (acétyl-CoA), d’autre part. L’avancée majeure de cette étude réside aussi bien dans la découverte d’un mécanisme de « dialogue métabolique-chromatine » pour l’adaptation environnementale, que dans le potentiel d’application offrant ainsi une nouvelle stratégie pour la sélection de variétés résistantes à la chaleur. -> Contact : dao-xiu.zhou@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
December 3, 6:08 AM
|
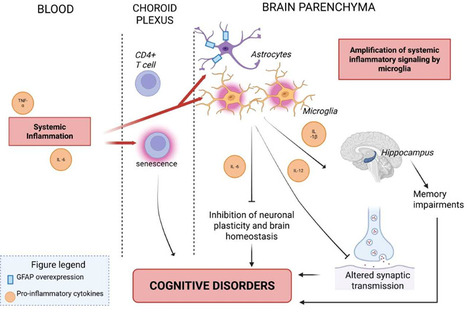
Dans une revue narrative récemment publiée dans Autoimmunity Reviews, les équipes du service de Médecine Interne et d’Immunologie Clinique de l’hôpital Bicêtre (AP-HP) et de l’UMR-S 1184, IMVA-HB (Center for Immunology of Viral Infections and Autoimmune Diseases, INSERM/CEA/UPSaclay, Le Kremlin Bicêtre) synthétisent les connaissances actuelles sur les troubles cognitifs observés dans plusieurs maladies auto-immunes et inflammatoires systémiques, un domaine encore largement sous-diagnostiqué. L’analyse de la littérature montre que ces troubles sont fréquemment rapportés dans certaines maladies systémiques telles que les vascularites associées aux ANCA, la maladie de Sjögren, la sclérodermie systémique, la sarcoïdose et la maladie de Behçet. Souvent d’origine dysexécutive ou attentionnelle, ils peuvent survenir même en l’absence d’atteinte neurologique objectivée, suggérant l’implication de mécanismes inflammatoires persistants. Leur dépistage reste difficile, faute d’outils standardisés et parce que les patients expriment rarement des plaintes cognitives spontanées. Sur le plan physiopathologique, la revue met en évidence le rôle central de l’inflammation chronique, qui perturbe le dialogue neuro-immun et peut altérer la plasticité neuronale et la transmission synaptique. Les altérations microvasculaires, les comorbidités psychiatriques et certains auto-anticorps peuvent également contribuer aux troubles cognitifs. Des techniques d’imagerie fonctionnelle et des biomarqueurs émergents, encore peu exploités en clinique, offrent de nouvelles perspectives pour mieux comprendre le retentissement cognitif de ces maladies. Ce travail insiste sur la nécessité d’une vigilance clinique accrue. La prise en compte des comorbidités et l’orientation vers une évaluation neuropsychologique lorsque nécessaire sont essentielles pour améliorer la prise en charge. Le développement de protocoles d’évaluation adaptés facilitera l’intégration de l’évaluation cognitive dans la pratique clinique et améliorera la qualité de vie des patients. -> Contact : nicolas.noel@aphp.fr

|
Scooped by
Life Sciences UPSaclay
December 3, 5:32 PM
|
Dans une étude intégrative publiée dans Journal of Investigative Dermatology, les scientifiques de l’équipe Génomique Translationnelle du Cancer dirigée par Sergey Nikolaev au sein de l'UMR-S 981 (Inserm/UPSaclay/Gustave Roussy, Villejuif), en collaboration avec l'équipe du Professeur Daniel Hohl au CHUV (Lausanne, Suisse), ont analysé le paysage moléculaire de 50 tumeurs issues du Syndrome Cutané de CYLD (CCS), un trouble génétique rare. Ces tumeurs, caractérisées par une très faible charge mutationnelle, présentent des mutations des gènes CYLD, DNMT3A et BCOR. Le travail a révélé une vulnérabilité oncogénique majeure et précise dans les cylindromes, les tumeurs caractéristiques du CCS : l'activation spécifique de la voie NF-κB non canonique. Cette activation, confirmée par des analyses d'expression et immunohistochimiques (forte expression nucléaire de NFKB2/p52), met en lumière un moteur essentiel de la formation tumorale. L’identification de cette branche non canonique ouvre la voie à l'exploration de thérapies ciblées, une avancée significative par rapport à l’échec des inhibiteurs non spécifiques du NF-κB testés antérieurement. De plus, le profilage par méthylation a résolu l’énigme de l’origine cellulaire de ces tumeurs. Les cylindromes (Groupe 1) proviennent des glandes sudoripares apocrines, tandis que les trichoépithéliomes (Groupe 2) se regroupent avec le carcinome basocellulaire (BCC). Ces résultats démontrent que la cellule d’origine dicte le phénotype tumoral, malgré la même mutation initiale de CYLD, et soulignent la nécessité de cibler l'axe NF-κB non canonique pour le traitement du CCS. -> Contact : sergey.nikolaev@gustaveroussy.fr

|
Scooped by
Life Sciences UPSaclay
December 4, 5:07 AM
|
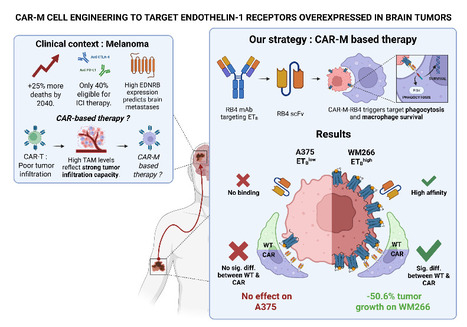
Les lymphocytes T génétiquement modifiés avec un récepteur antigénique chimérique (CAR-T) contenant un fragment d’anticorps afin de cibler la réponse immunitaire sur les cellules tumorales ont donné des résultats impressionnants dans le traitement des tumeurs hématologiques. Ces traitements permettant d’obtenir jusqu’à 83% de rémission sur la leucémie lymphoblastique, ont malheureusement montré une efficacité plus limitée dans le cadre de tumeurs solides en raison de la présence d’un microenvironnement immunosuppresseur. Les macrophages, puissantes cellules du système immunitaire, sont fortement recrutés au sein des tumeurs solides où ils vont exercer sous l’influence du microenvironnement une activité pro-tumorale. Dans une étude publiée dans Cancer Immunology, Immunotherapy, une équipe du laboratoire d'Étude de l'Unité Neurovasculaire & Innovation Thérapeutique - LENIT (SPI/DMTS CEA/UPSaclay, Gif-sur-Yvette) a étudié l’impact de macrophages modifiés avec le fragment d’anticorps Rendomab B4 (CAR-M-RB4) sur des cellules tumorales surexprimant le récepteur des endothélines de type B (ETB) ciblées par le CAR-M-RB4. La spécificité de l’anticorps RB4 pour ETB a été combinée à des domaines d’activation intracellulaire pour réorienter et amplifier la réponse antitumorale. Lors de leur étude sur la croissance de différentes lignées de cellules issues de mélanomes métastatiques de patients, les chercheurs ont montré que le CAR-M-RB4 ciblait efficacement les cellules de mélanome ETB+ et réduisait de 50% leur croissance dans les modèles de culture 2D et 3D. A l’inverse, aucun effet n’a été observé sur les cellules de mélanome ETB-, démontrant une activité spécifique de l’antigène cible. Dans leur ensemble, ces résultats soulignent le fort potentiel thérapeutique du CAR-M RB4 pour le traitement des tumeurs ETB+. -> Contact : didier.boquet@cea.fr

|
Scooped by
Life Sciences UPSaclay
December 7, 9:01 AM
|
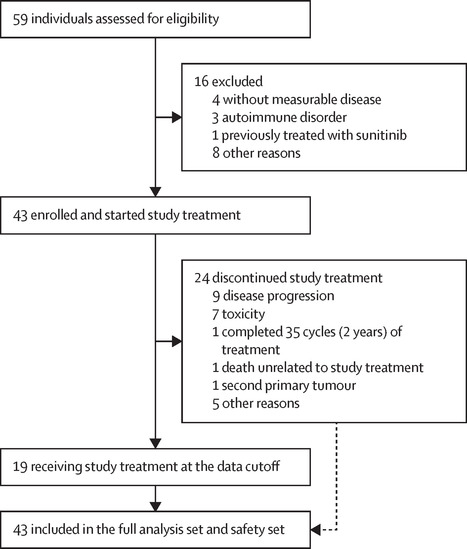
Les cancers du thymus, localisés sur une petite glande située dans la partie supérieure du thorax, sont rares. Pour les patients porteurs d’un thymome de type B3 avancé ou d’un carcinome thymique, deux sous-types de la maladie, il n’existe malheureusement pas de standard thérapeutique après l’échec des traitements à base de platine. Un article paru dans The Lancet Oncology relate les résultats de l’essai de phase II PECATI, toujours en cours, sur des patients porteurs de ces indications recrutés dans 11 hôpitaux en France, en Italie et en Espagne. L’objectif de cet essai, coordonnée par Benjamin Besse (Gustave Roussy, Villejuif), est d’évaluer l’activité antitumorale et la sécurité du lenvatinib, une thérapie ciblée qui empêche la tumeur de créer de nouveaux vaisseaux sanguins, associé au pembrolizumab, une immunothérapie. Les participants avaient tous vu leur maladie progresser après un premier cycle de chimiothérapie à base de platine. Après un premier suivi, l’étude a atteint son objectif principal, puisque 88,4% des patients n'avaient pas vu leur maladie progresser à cinq mois, avec des effets indésirables observés. Ces résultats suggèrent que l’association lenvatinib-pembrolizumab pourrait constituer une nouvelle option thérapeutique pour ces patients en impasse, sous réserve d’une surveillance étroite des toxicités. -> Contact : jordi.remon-masip@gustaveroussy.fr

|
Scooped by
Life Sciences UPSaclay
December 7, 9:33 AM
|
Raphaël Mercier reçoit le prestigieux prix VinFuture pour ses travaux sur la reproduction clonale par graine Ancien responsable de l'équipe MeioMe et aujourd’hui directeur au Max Planck Institute, Raphaël Mercier reçoit le Prix spécial d’innovation VinFuture 2025 pour des travaux initiés à l’Institut Jean-Pierre Bourgin - Sciences du Végétal - IJPB (INRAE/AgroParisTech/UPSaclay, Versailles). Cette distinction de la fondation VinFutur lui a été remise le 5 décembre 2025 à Hanoï (Vietnam) lors d’une cérémonie honorant des avancées scientifiques et technologiques susceptibles de simplifier la propagation des variétés élites de plantes cultivées, révolutionnant ainsi l’agriculture et contribuant de façon significative à la sécurité alimentaire. Lire la suite de l’Actu IJPB
|






 Your new post is loading...
Your new post is loading...