Your new post is loading...

|
Scooped by
Life Sciences UPSaclay
October 29, 2018 8:39 AM
|
La conception de médicaments à cibles multiples présente des avantages considérables dans le traitement de maladies complexes telles que le cancer. Leur conception est considérée comme un défi pour la découverte de médicaments antitumoraux. Dans ce contexte, des chercheurs de l’équipe CosMIT (BioCIS – CNRS/UPSud UMR 8076) ont conçu et synthétisé des molécules duales qui sont à la fois inhibitrices de la polymérisation de la tubuline ainsi que de l’activité des histones désacétylases. Ces travaux, publiés dans le journal Journal of Medicinal Chemistry, portent sur la synthèse d’une nouvelle série de molécules hybrides sur la base de l’isocombrétastineA-4 et du bélinostat. Ces molécules se sont avérées être de puissants inhibiteurs de la polymérisation de la tubuline et de HDAC8 conduisant à une excellente activité anti-proliférative. Contact : abdallah.hamze@u-psud.fr

|
Scooped by
Life Sciences UPSaclay
October 9, 2018 5:10 PM
|
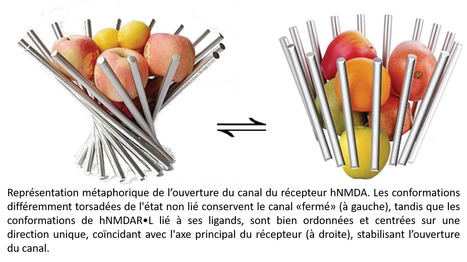
Les récepteurs NMDA (NMDAR) jouent un rôle primordial dans le système nerveux central, contribuant à la plasticité synaptique, la base fondamentale des processus d’apprentissage et de mémorisation. L’activation du NMDAR par ses ligands, glutamate (E) et glycine (G), déclenche l'ouverture d'un canal ionique perméable aux cations (sodium, potassium, et calcium). La sur-activation du récepteur NMDA, en provoquant un afflux excessif d’ions Ca2+, peut générer une forme d’excitotoxicité impliquée dans certaines maladies neurodégénératives. À l’inverse, un hypofonctionnement des récepteurs NMDA peut altérer la plasticité synaptique. Ces récepteurs sont par ailleurs présents dans des systèmes périphériques non neuronaux et impliqués dans de nombreux autres processus pathologiques, comme le cancer, le diabète ou en encore l’hypertension artérielle pulmonaire (HTAP), une maladie mortelle pour laquelle il n’existe pas de traitement curatif, et qui a fait l’objet de l’ANR NUTS 2014-2018, coordonnée par Sylvia Cohen-Kaminsky (INSERM/UPSud UMR-S 999, LabEx LERMIT, DHU TORINO). Outre valider le NMDAR comme nouvelle cible thérapeutique dans l’HTAP (Article dans Circulation 2018), et développer de nouveaux composés antagonistes des NMDAR périphériques qui ne passent pas la barrière hémato-encéphalique (BHE), le projet NUTS avait également comme ambition de générer un modèle moléculaire dynamique tout atome du NMDAR, qui puisse être à terme utilisé pour la découverte de nouveaux antagonistes. La complexité de la structure des récepteurs NMDA (un tétramère composé de 4 sous-unités moléculaires de 800-900 résidus chacune), et les difficultés de leur étude expérimentale, font de ces récepteurs membranaires un paradigme pour la modélisation. Dans le cadre du projet NUTS, l’équipe de Luba Tchertanov (CMLA - ENS Paris-Saclay) a relevé ce défi, et a modélisé la structure du NMDAR humain (hNMDAR) et étudié ses propriétés dynamiques et énergétiques, par la simulation de la dynamique moléculaire de deux modèles : hNMDAR-L et hNMDAR, liés et non liés avec ses ligands glycine et glutamate (L= E et G). Dans un article qui vient de paraitre dans PLoS One, à partir de ces données de simulation, l’équipe a mis en évidence les effets induits par la fixation des ligands sur la plasticité conformationnelle du récepteur, qui se traduisent par une réduction globale de la flexibilité moléculaire et une plus grande régularité et coopérativité dans le déplacement atomique. L’étude montre que la synchronisation du mouvement induite par les ligands à tous les niveaux structurels du hNMDAR modulaire, est apparemment un facteur fondamental, requis pour l’ouverture du canal. Pour la première fois, un modèle dynamique du mécanisme d’ouverture du canal du récepteur NMDAR humain est proposé, avec une nouvelle vision de l’ouverture du canal ionique par la fixation de ses ligands. Lors de la liaison des ligands, les différentes conformations torsadées du récepteur hautement flexible sont stabilisées dans une conformation unique avec un axe moléculaire linéaire, ce qui est optimal pour le développement du canal. Par ailleurs, en examinant la surface du récepteur, l’équipe a identifié trois nouvelles poches, jusqu’ici non décrites dans la littérature comme sites de liaison potentiels de modulateurs allostériques positifs connus, validant ainsi ce modèle. La prochaine étape sera de tester la possibilité d’utiliser ce modèle pour le criblage in silico des nouveaux antagonistes des NMDARs ne passant pas la BHE, mis au point et produits en collaboration avec Mouad Alami (BioCIS, CNRS UMR 8076, Faculté de Pharmacie Paris-Sud) et Alain Pruvost (CEA, LEMM), dans le cadre du LabEx LERMIT et de la SATT Paris Saclay (projet NUTS-MAT), pour le traitement de maladies périphériques impliquant le NMDAR, comme l’Hypertension Artérielle Pulmonaire. Le développement de ce projet à l’interface - Biologie-Santé / Chimie Médicinale / Mathématiques appliquées - est un bel exemple de collaboration pluridisciplinaire au sein de l’Université Paris-Saclay. Contact : luba.tchertanov@ens-cachan.fr ou sylvia.cohen-kaminsky@u-psud.fr

|
Scooped by
Life Sciences UPSaclay
July 12, 2018 6:26 PM
|
Le monde végétal inspire constamment la chimie, mais comment faire lorsqu’une plante d’intérêt ne vit en symbiose que dans un seul endroit reculé ?
L’algue Amphidinium cohabite ainsi avec une bactérie uniquement dans la baie japonaise d’Okinawa, où ils produisent une famille de molécules cytotoxiques pouvant servir en chimiothérapie anticancéreuse : les amphidinolides.
Des chercheurs du laboratoire BioCIS (CNRS/Université Paris-Sud/Université Paris-Saclay - Faculté de Pharmacie, Châtenay-Malabry) se sont intéressés à cette algue et sont parvenus, en vingt-trois étapes, à synthétiser totalement l’amphidinolide F. Ces travaux sont publiés dans Organic Letters. Contact: laurent.ferrie@u-psud.fr ou bruno.figadere@u-psud.fr

|
Scooped by
Life Sciences UPSaclay
June 21, 2018 6:10 PM
|
Pour marquer les 20 ans de l’European Journal of Organic Chemistry, le laboratoire Biomolécules Conception, Isolement, Synthèse (UPSud/CNRS) de la faculté de Pharmacie de l’Université Paris-Sud est présent avec une publication dans le volume spécial commémorant l’évènement.

|
Scooped by
Life Sciences UPSaclay
February 7, 2018 1:10 PM
|
Les allergies médicamenteuses représentent un problème majeur de santé publique et la majorité est due à des antibiotiques tels que les bêta-lactamines. Les composés chimiques, tels que la benzylpenicilline (BP), sont des molécules de faible poids moléculaire qui ne peuvent être reconnus par le système immunitaire et ne peuvent donc pas déclencher une réponse immunitaire adaptative. Ainsi pour devenir immunogène, ces molécules se lient à des protéines telles que l’albumine humaine (HSA). Le complexe ainsi formé est internalisé par les cellules présentatrices d’antigène qui présentent ensuite des conjugués peptides-molécules, associés aux molécules HLA, aux lymphocytes T (LT). Dans une étude à paraitre dans Allergy, Marc Pallardy et son équipe à la Faculté de Pharmacie de Châtenay-Malabry (Unité INSERM/UPSud UMR-S 996, en collaboration avec l'uMR 8076 BioCIS CNRS/UPSud et le SIMOPRO du CEA de Saclay - LabEx LERMIT), apportent une compréhension des mécanismes de l’immunisation contre les médicaments et le rôle des LT dans le développement des allergies médicamenteuses. Les chercheurs ont mis en évidence l'existence d’un répertoire de LT naïfs CD4+ spécifiques du bioconjugué HSA-BP chez des donneurs sains ( http://onlinelibrary.wiley.com/doi/10.1111/all.12173/abstract). Ensuite, ils se sont intéressés à l’identification des peptides haptenisés par la BP, issus de la HSA, et impliqués dans l’activation des LT naïfs ainsi que dans l’immunisation des patients allergiques. Leur stratégie a permis (1) l’identification des résidus lysine présents sur la HSA hapténisés par la BP par spectrométrie de masse, (2) la sélection par une approche in silico des peptides de 15-mer potentiellement immunogènes, (3) la synthèse orientée de ces peptides-BP à l’aide d’un monomère lysine-BP ( https://pubs.acs.org/doi/10.1021/acs.bioconjchem.6b00393), (4) l’identification des épitopes reconnus par les LT naïfs de donneurs sains grâce à un modèle de co-culture autologue DC-LT, (5) la validation de deux épitopes situés sur les lysines 159 et 525 chez les patients allergiques aux pénicillines. D’une manière générale, ce projet a permis, d’une part, l’identification d’épitopes impliqués dans l’immunisation à la BP pouvant servir dans le développement d’un test à visée diagnostic et, d’autre part, d’établir une stratégie de prédiction de peptides potentiellement immunogènes. Contact : marc.pallardy@u-psud.fr

|
Scooped by
Life Sciences UPSaclay
June 1, 2017 4:22 PM
|
Mouad ALAMI, lauréat 2017 du Prix du Conseil Départemental des Yvelines de la Ligue contre le Cancer
Le Comité Départemental de la Ligue pour les Yvelines remet tous les ans un prix à deux chercheurs reconnus. Ce prix, d’un montant de 12 500 euros pour chaque équipe, est abondé par le Conseil Général du Département des Yvelines. Le Conseil Scientifique national de la Ligue contre le cancer a désigné notre collègue Mouad ALAMI, Directeur de Recherche CNRS, responsable du Laboratoire Conception et Synthèse de Molécules d'Intérêt Thérapeutique (CoSMIT) au sein de l'UMR CNRS/UPSud/UPSaclay 8076 BioCIS (Faculté de Pharmacie de Châtenay-Malabry) Lauréat du Prix 2017 pour ses travaux de recherche.
Félicitations pour cette haute distinction !

|
Scooped by
Life Sciences UPSaclay
March 16, 2017 7:21 AM
|
Un consortium rassemblant des chercheurs de plusieurs équipes du CNRS (BioCIS, UFR Pharmacie, Uinv Paris-Sud, Châtenay-Malabry), du CEA (IbitecS, Saclay), de plusieurs universités Italiennes et coordonné par l’Institut Galien Paris-Sud (UPSud/CNRS) s’est donné pour objectif de mettre au point de nouveaux candidats médicaments pour prévenir et traiter plus efficacement les infections microbiennes qui atteignent la peau et les muqueuses. « Notre stratégie consiste à faire appel à la formulation pour booster l’efficacité de molécules antimicrobiennes. Ces candidats médicaments seront donc moins toxiques, mieux tolérés et le risque de résistance sera diminué. L’étude des synergies entre les composants de ces formulations est un axe majeur de notre activité de recherche » a déclaré Kawthar Bouchemal, Maître de Conférences à l’Institut Galien Paris Sud (UPSud/CNRS), et membre junior de l’Institut Universitaire de France.
Contact: kawthar.bouchemal@u-psud.fr
|

|
Scooped by
Life Sciences UPSaclay
October 23, 2018 10:25 AM
|
Dans le cadre d’une collaboration entre le laboratoire Biomolécule-Conception, Isolement et Synthèse (BioCIS – CNRS/UPSud UMR 8076) et le Centre de Biophysique Moléculaire (CBM – CNRS UPR 4301 Orléans), des chercheurs ont mis au point une méthode originale pour synthétiser des peptides thioglycosylés, des glycoconjugués très stables dans les milieux biologiques. Ces travaux publiés dans la revue Chemical Science représentent une avancée notable en glycochimie et ouvrent la possibilité à de multiples applications dans la synthèse de glycopeptides et glycoprotéines d’intérêt thérapeutique ou en tant qu’outils pour explorer le monde du vivant. Contact : samir.messaoudi@u-psud.fr

|
Scooped by
Life Sciences UPSaclay
September 6, 2018 4:31 AM
|
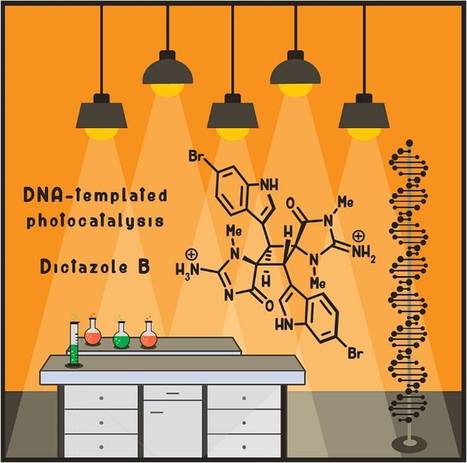
Offrant des possibilités uniques de confinement dans un environnement chiral, la catalyse à base d’ADN se développe en synthèse organique depuis quelques années. Un article dans la revue Angewandte Chemie repousse les frontières de l’utilisation de l’ADN à plusieurs égards. Des réactions photochimiques de dimérisation en présence d’ADN ont été étudiées et optimisées, elles permettent ici d’effectuer en solution des cycloadditions [2+2] jusque là uniquement réalisables à l’état solide. Ainsi, au départ de substances naturelles d’origine marine – les aplysinopsines – des composés à architectures tridimensionnelles complexes sont formés avec d’excellents rendements en présence d’ADN. Pour finaliser le tout, c’est même une hétérodimérisation conduisant spontanément à une substance naturelle – le dictazole B – qui a pu être réalisée dans l’environnement particulier des sillons de l’ADN chargés négativement. Les expériences ont été menées dans des conditions recréant un ensoleillement intense et permettent, sur la base d’hypothèses de biosynthèse, de proposer dans ce travail la première synthèse totale bio-inspirée en présence d’ADN. Ce travail a été effectué par un consortium de deux équipes françaises (BioCIS, CNRS/UPSud, Faculté de Pharmacie, Châtenay-Malabry, et Université de Montpellier) et une équipe britannique (Queen Mary University of London) et dans le cadre d'un projet financé par le LabEx LERMIT. Contacts : erwan.poupon@u-psud.fr, laurent.evanno@u-psud.fr , michael.smietana@umontpellier.fr et s.arseniyadis@qmul.ac.uk

|
Scooped by
Life Sciences UPSaclay
June 23, 2018 5:10 PM
|
En juin 2018, le fruit d’un travail collaboratif entre l’Institut Galien Paris-Sud (Félix Sauvage, Juliette Vergnaud-Gauduchon, Elias Fattal, Gillian Barratt) et BioCIS (Samir Messaoudi, Mouad Alami), de la Faculté de Pharmacie de l’Université Paris-Sud a été publié dans la revue Cancer Letters. Les auteurs ont identifié le potentiel anti-tumoral de liposomes encapsulant un inhibiteur potentiel de la protéine de choc thermique Hsp90 au niveau de son domaine C-terminal (6BrCaQ, analogue de la novobiocine). Tout d’abord, la réponse cellulaire in vitro à ces liposomes a été caractérisée sur la lignée de cancer du sein MDA-MB-231 : un ralentissement de la prolifération cellulaire a été observé sans induction d’une réponse Heat Shock, observée notamment avec les inhibiteurs N-terminaux de Hsp90 et responsable de la résistance au traitement. Dans un modèle de xénogreffe orthotopique de cancer du sein bioluminescent chez la souris nude (MDA-MB-231-Luc), le 6BrCaQ liposomal, administré une fois par semaine par voie intra-veineuse à 1 mg/kg pendant 4 semaines, induit un ralentissement de la croissance tumorale mesurée par l’activité luciférase et le volume tumoral. Cet effet apparaît plutôt lié à une inhibition de la prolifération des cellules tumorales évaluée par un marquage histologique au Ki67 que par l’induction d’apoptose (marquage de la caspase-3 clivée). Cette étude montre avec succès la possibilité de délivrer in vivo, grâce à des liposomes, un inhibiteur C-terminal de l’Hsp90 très peu soluble dans les milieux biologiques et ainsi de faciliter son développement éventuel en tant que candidat médicament. Contact : juliette.vergnaud@u-psud.fr

|
Scooped by
Life Sciences UPSaclay
June 8, 2018 5:27 PM
|
Pour marquer les 20 ans de l’European Journal of Organic Chemistry, le laboratoire Biomolécules Conception, Isolement, Synthèse (UPSud/CNRS) de la faculté de Pharmacie de l’Université Paris-Sud, rattachée au Département SDV de l'UPSaclay, est présent avec une publication dans le volume spécial commémorant l’évènement.

|
Scooped by
Life Sciences UPSaclay
December 7, 2017 4:08 AM
|
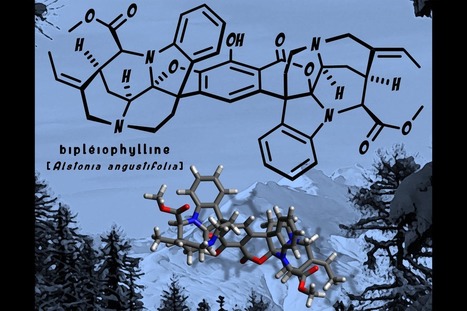
Guidé par une passion de longue date pour les molécules présentant une activité biologique, Adam Skiredj a suivi un double cursus en pharmacie industrielle et chimie médicinale. Il a ensuite réalisé un doctorat en chimie sous la direction du Professeur Erwan Poupon (BioCIS, UMR 8076, Faculté de Pharmacie, UPSud, Châtenay-Malabry) financé par le LabEx LERMIT. L'objectif de sa thèse était la synthèse biomimétique de substances naturelles complexes. Son travail a été couronné par le Prix Régnier de la Chancellerie des Universités de Paris.
Toutes nos félicitations !

|
Scooped by
Life Sciences UPSaclay
March 16, 2017 7:28 AM
|
Un travail de collaboration entre des équipes (CNRS – Université Paris-Sud - Université Paris-Saclay - LabEx LERMIT) de l’ICMMO (Institut de Chimie Moléculaire de des Matériaux d’Orsay, UFR des Sciences) et de BioCIS (Biomolécules : Conception, Isolement, Synthèse, UFR de Pharmacie de Châtenay-Malabry) publié dans la revue Nature Chemistry a permis de montrer qu’il était possible d’assembler des architectures moléculaires incroyablement complexes au laboratoire.
Lien vers article: http://www.nature.com/nchem/journal/vaop/ncurrent/full/nchem.2735.html
|



 Your new post is loading...
Your new post is loading...