Your new post is loading...

|
Scooped by
Life Sciences UPSaclay
March 9, 2021 5:06 PM
|
La maladie de Charcot-Marie Tooth est la maladie neurologique héréditaire la plus fréquente au monde. Elle touche le nerf périphérique et entraine une paralysie progressive des jambes et des mains. Aucun traitement n’est aujourd’hui disponible pour lutter contre cette maladie, due à la surexpression d’une protéine spécifique. Des scientifiques du CNRS, de l’Inserm, de l’AP-HP et des universités Paris-Saclay (UMR-S 1195 Inserm/UPSaclay, Le Kremlin-Bicêtre ; UMR 9018 CNRS/UPSaclay/Gustave Roussy, Villejuif; Institut Galien Paris-Saclay UMR 8612 CNRS/UPSaclay, Châtenay-Malabry ; Service de neurologie - centre de référence national des neuropathies amyloïdes familiales et autres neuropathies périphériques rares du CHU du Kremlin-Bicêtre, AP-HP/UPSaclay) et de Paris ont mis au point, chez la souris, une thérapie fondée sur la dégradation de l’ARN codant pour cette protéine. Leurs travaux, brevetés, sont publiés le 9 mars 2021 dans Communications Biology. Légende Figure : Nanoparticule siRNA PMP22-squalène. Lire le communiqué de presse ICI. Contact : liliane.massade@inserm.fr

|
Scooped by
Life Sciences UPSaclay
February 13, 2021 12:58 PM
|
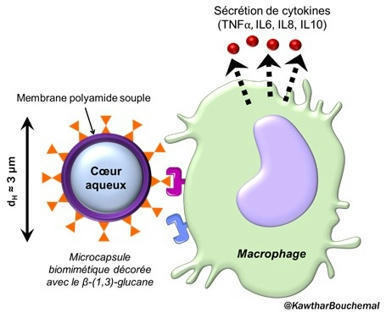
L’inhalation par l’Homme des spores disséminées dans l’air du champignon Aspergillus fumigatus peut conduire à des maladies pulmonaires parfois mortelles. Des recherches ont montré que la couche externe de ces spores, essentiellement constituée de sucres, participait à l’élimination du pathogène. D’où l’intérêt d’identifier le rôle de chaque sucre dans l’induction de la réponse immunitaire de l’hôte. En concevant des microcapsules biomimétiques sur lesquelles ils ont greffé différents polysaccharides, les scientifiques de l’Institut Galien Paris Saclay - IGPS (CNRS/Université Paris-Saclay, Châtenay-Malabry) et de l’Institut Pasteur à Paris sont parvenus à mieux comprendre l’effet immunomodulateur des sucres de la paroi des champignons. Résultat à retrouver dans la revue Bioconjugate Chemistry. Lire la suite ICI. Contact : kawthar.bouchemal@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
December 8, 2020 4:51 AM
|
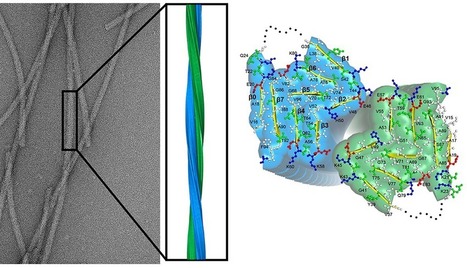
L’agrégation intra-neuronale de la protéine Tau sous forme d’assemblages fibrillaires est intimement associée à des maladies neurodégénératives incurables connues sous le nom de Tauopathies qui comptent parmi elles la maladie d’Alzheimer. Nos neurones expriment 6 isoformes différentes de cette protéine de 352 à 441 acides aminés. De plus, l’agrégation de différentes isoformes caractérisent des tauopathies distinctes. Les équipes de Physico-Chimie des Surfaces de l'Institut Galien (UMR 8612, CNRS/UPSaclay/LabEx LERMIT, Châtenay-Malabry) et Agrégation des protéines et maladies neurodégénératives du laboratoire des maladies neurodégénératives (MIRCen CNRS/CEA-Jacob/UPSaclay, Fontenay-aux-Roses) ont caractérisé les propriétés structurales, morphologiques et nano-mécaniques des formes fibrillaires pathogéniques des 6 isoformes de la protéine Tau par microscopies électronique et à force atomique (ME et AFM). Leur étude, parue dans dans Biophysical Journal, montre que tous les assemblages fibrillaires de Tau sont constitués de deux protofilaments. De plus, les fibrilles composées de molécules de Tau comportant quatre domaines (4R) de liaison aux microtubules ont une longueur de persistance deux fois plus élevée que celles avec trois domaines (3R). Les modules de Young axiaux et radiaux mesurés sont nettement inférieurs à ceux d'autres assemblages amyloïdes. Cela suggère que les interactions intermoléculaires entre les feuilles β au sein des fibrilles de Tau sont faibles. Ces résultats montrent pour la première fois que les fibrilles de Tau sont fragiles. Cette fragilité joue certainement un rôle majeur dans leur propagation et multiplication à la manière du prion. Contact : ali.makky@universite-paris-saclay.fr ou ronald.melki@cnrs.fr

|
Scooped by
Life Sciences UPSaclay
November 15, 2020 1:06 PM
|
Depuis 2010, la plateforme d'interactions moléculaires (INTERMOL) fait partie de l’UMS IPSIT (INSERM/CNRS/UPSaclay, Faculté de Pharmacie, Châtenay-Malabry) et offre régulièrement ses services aux équipes de recherche académiques du territoire Paris-Saclay – et notamment celles impliquées dans l'innovation thérapeutique – en proposant son expertise technique et scientifique. La plateforme assure régulièrement des prestations pour des partenaires académiques extérieurs ou privés, et est membre du Réseau européen ARBRE - Association of Ressources for Biophysical Research in Europe. INTERMOL dispose tout particulièrement d’un Biacore® T100 (Cytiva) et maitrise la technologie de résonance plasmonique de surface (SPR), équipement et méthodologie permettant de caractériser finement l'affinité d'interaction entre 2 partenaires (KD) mais aussi d'en évaluer les constantes cinétiques et ainsi mieux comprendre le mécanisme d'interaction. La haute sensibilité de cet équipement permet aussi de travailler avec des molécules de très faible poids moléculaire (300 Da), ce qui concerne de nombreux candidats médicaments. Exemple choisi de développement, dans le cadre d’une collaboration avec l'Institut Galien Paris-Saclay (UMR CNRS 8612): L'Institut Galien Paris-Saclay (UMR CNRS 8612) a notamment pour mission de concevoir, de préparer et de caractériser des nanomédicaments capables d'optimiser l'activité pharmacologique des substances actives, en les protégeant par encapsulation lorsqu'elles sont fragiles, en améliorant leur passage à travers les barrières biologiques et en ciblant leur site d'action afin de diminuer les effets indésirables. Dans ce cadre, les interactions moléculaires jouent un rôle central et la caractérisation de ces interactions entre formulations innovantes et cible thérapeutique est essentielle. Lors de la conception de lipoplexes fonctionnalisés avec des fragments d'acide hyaluronique, destinés à cibler les récepteurs CD44 présents sur de nombreuses cellules tumorales, INTERMOL a mis au point une méthode SPR spécifique adaptée aux contraintes particulières des structures supramoléculaires (interactions multivalentes, phénomène de transfert de masse, avidité). Cette méthodologie a permis une caractérisation précise de l'interaction moléculaires entre les lipoplexes et le récepteur CD44 (voir figure ci-dessus). Les outils de microcalorimétrie également disponibles sur INTERMOL ont en outre permis de caractériser l'encapsulation d'ARN interférents (siRNA) dans ces lipoplexes dans une perspective de thérapie génique anticancéreuse. En savoir plus ? Nascimento et al., Langmuir 2015. D’autres projets comme la mise au point de fragments d'anticorps thérapeutiques (Fogaça et al., Nanomedicine 2019) ou la sélection de protéines recombinantes (Vidic et al., Biochemistry 2016) ont également été conduits par la plateforme grâce à la technique SPR, permettant de caractériser leur affinité pour leur cible thérapeutique et optimiser leur séquence. Contact : Magali Noiray (magali.noiray@universite-paris-saclay.fr) Plug In Labs Université Paris-Saclay : cliquer ici IPSIT / plateforme interactions moléculaires (INTERMOL). Les interactions moléculaires jouent un rôle central dans le monde vivant, qu’il s’agisse d’interactions entre des protéines, des glycoprotéines, des lipoprotéines ou encore entre des molécules d’ADN ou d’ARN. Dans le domaine pharmaceutique, la connaissance des interactions entre ces macromolécules et des molécules d’intérêt pharmaceutique, généralement de plus petite taille est essentielle pour concevoir de nouveaux médicaments. L’objectif de la plateforme "Interactions Moléculaires" est de proposer des techniques d’études complémentaires adaptées à l’étude fine de ces interactions. A l’heure actuelle, la plateforme se compose d’un équipement de résonance plasmonique de surface (SPR) de type Biacore T100 (GE Healthcare). Des techniques complémentaires telles que la titration calorimétrique iso-thermique (ITC), la calorimétrie différentielle à balayage (DSC), une microbalance à quartz (QCM) ou encore de la microscopie à fluorescence sont également disponibles sur le site de la Faculté de Pharmacie de Châtenay-Malabry. En partenariat avec la plateforme Transcriptomique TRANS-PROT de l'IPSIT, une nouvelle activité se développe: la plateforme propose d'étudier la stabilité des protéines, partenaires d'interactions, et de mettre en évidence leurs interactions avec des ligands. L'appareil de SPR est ouvert à l'ensemble des laboratoires de la Faculté de Pharmacie, Université Paris Saclay, des autres laboratoires académiques ainsi que les industriels.

|
Scooped by
Life Sciences UPSaclay
October 6, 2020 7:51 AM
|
L’immunogénicité des biothérapies constitue une limitation majeure au traitement des patients atteints de maladies chroniques et se traduit par la production d’anticorps dirigés contre le biomédicament (anti-drug antibodies, ADA). La détection d’ADA de haute affinité et d’isotypes divers chez les patients suggère la mise en place d’une réponse immunitaire adaptative classique orchestrée par les cellules dendritiques. Par ailleurs, la présence d’agrégats protéiques dans les spécialités administrées serait un des facteurs favorisant l’immunogénicité, ces agrégats pouvant jouer le rôle de signal de danger reconnu par les cellules dendritiques. Dans une étude récente parue dans Journal of Immunology, des chercheurs de l’UMR-S 996 (Inserm/UPSaclay, Châtenay-Malabry), en collaboration avec des chercheurs de l’Institut Galien Paris-Saclay (CNRS, UPSaclay, Châtenay-Malabry), ont évalué les mécanismes cellulaires précoces de la réponse immunitaire aux agrégats d’un anticorps monoclonal anti-TNFα, l’infliximab. En effet, ces agrégats induisaient la maturation de cellules dendritiques humaines dérivées de monocytes qui à leur tour favorisaient la prolifération de lymphocytes T CD4+ et la production de cytokines. Les résultats de cette étude mettent en évidence que l’activation de ces cellules immunitaires en réponse aux agrégats d’infliximab est dépendante du récepteur FcγRIIa et de la tyrosine kinase Syk. In fine, ce travail contribue à une meilleure compréhension des conséquences biologiques de l’agrégation des protéines à visée thérapeutique sur le déclenchement de la réponse immunitaire adaptative spécifique en mettant l’accent sur le rôle adjuvant des agrégats d’anticorps. Contact : isabelle.turbica@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
June 18, 2020 6:01 PM
|
Le tactisme (taxie), déplacement orienté en réponse à un stimulus externe, aide certains organismes à migrer, à se nourrir ou à éviter certains dangers. En imitant le tactisme naturel, de nombreux transporteurs de médicaments bio-inspirés ont été synthétisés. Sous l’influence de stimuli, ces transporteurs sont dirigés vers des cellules cibles, par exemple tumorales, permettant de focaliser leur action. Cette mobilité orientée nécessite de doter les vecteurs de fonctionnalités leur permettant de répondre à des stimuli physiques (champ magnétique ou électrique, …) ou chimiques (micromoteurs, vecteurs bio-hybrides…). Symétriquement, il est possible d’envisager le déplacement de la cible, par exemple une cellule métastatique ou une bactérie, lorsque celle-ci présente un tropisme particulier pouvant être mis à profit pour une action thérapeutique. Par exemple, plusieurs pièges et niches biologiques ont été étudiées dans la littérature pour attirer, puis éliminer, des cellules cancéreuses en libérant des chimiokines. Dans une revue qui vient de paraitre dans le Journal of Controlled Release, Hung V. Nguyen et Vincent Faivre de l’Institut Galien Paris-Sud (UMR 8612 CNRS/UPSaclay, Faculté de Pharmacie, Châtenay-Malabry) font le point sur les avancées et les limites de ces différentes approches. Contact : vincent.faivre@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
May 7, 2020 5:43 PM
|
Les cultures de cellules en deux dimensions (2D) sont très utilisées dans de nombreux domaines tels que la biologie cellulaire, l’évaluation de médicaments et la médecine régénérative. Elles ont en effet permis d’acquérir de précieuses connaissances concernant, par exemple, les mécanismes biologiques mis en jeu lors du développement cellulaire ou de la réponse cellulaire sous l’action de perturbations endogènes ou exogènes, ainsi que l’efficacité de nouveaux principes actifs et nanomédicaments, ou encore la morphogénèse tissulaire. Cependant, un tel environnement bidimensionnel ne reproduit pas fidèlement le microenvironnement naturel en trois dimensions (3D) que l’on retrouve in vivo où les cellules sont entièrement entourées d’autres cellules, de couches fibreuses et de protéines d’adhésion. On dénote alors en 2D l’absence de nombreuses interactions biologiques qui existent in vivo, ce qui conduit à des différences phénotypiques et génotypiques notables. Afin de recréer le microenvironnement, de nombreuses recherches se sont orientées vers le développement de matrices extracellulaires synthétiques en 3D. Un article de revue paru dans Biomacromolecules, écrit par des chercheurs de l’Institut Galien Paris-Saclay (IGPS, CNRS/Université Paris-Saclay, Faculté de Pharmacie, Châtenay-Malabry) et de l’Université de Milano-Bicocca, présente et détaille non seulement les caractéristiques chimiques et structurelles des différents matériaux utilisés pour concevoir des matrices extracellulaires synthétiques en 3D, mais également les biomolécules impliquées dans la signalisation et qui sont exploitées pour générer des microenvironnements capables d’induire un devenir cellulaire spécifique. Il présente également les différentes stratégies synthétiques impliquées dans la création de matrices extracellulaires synthétiques en 3D, mettant en exergue le rôle fondamental de la chimie des matériaux et plus spécifiquement des polymères dans ce domaine. Contact : julien.nicolas@universite-paris-saclay.fr ou laura.russo@unimib.it

|
Scooped by
Life Sciences UPSaclay
April 7, 2020 10:56 AM
|
Pseudomonas aeruginosa est l'un des plus virulents agents pathogènes causant des infections nosocomiales. Cette bactérie qui forme un biofilm est la principale menace pour la vie des patients atteints d’infections pulmonaires sévères comme la mucoviscidose. Protégée au sein de son biofilm, c'est l'une des bactéries les plus difficiles à traiter cliniquement. Un consortium européen Horizon 2020 impliquant l’équipe « Nanomédicaments pour le traitement de maladies graves » de l’Institut Galien Paris-Sud (UMR 8612 CNRS/UPSaclay, Faculté de Pharmacie, Châtenay-Malabry), l’Institut Helmholtz de Recherche Pharmaceutique (Saarbrucken, Allemagne), le Department of Bioengineering, School of Medicine de l’Université de Washington (USA), et le German Centre for Infection Research (DZIF, Saarbrucken, Allemagne) a récemment proposé d’éradiquer ces bactéries en mettant à profit la synergie entre un antibiotique de la famille des aminoglycosides : la tobramycine et une quinolone inhibitrice du quorum sensing décrite récemment par Anke Steinbach et Rolf W. Hartmann. Néanmoins la faible solubilité de cette molécule dans l’eau interdit une simple combinaison avec la tobramycine. Pour résoudre ce problème, Didier Desmaële et Patrick Couvreur ont réussi à encapsuler le mélange des deux principes actifs dans un nanovecteur constitué d’hydrogénosulfate de squalényle, les conjugués de squalène étant capables de s’autoassembler de manière spontanée comme déjà montré précédemment. Dans le cas présent, la charge négative portée par la tête polaire du vecteur squaléné permet une association optimale avec la tobramycine chargée positivement à pH physiologique, alors que la quinolone peut s’insérer dans les sites lipophiles offerts par les chaines squalène. Ces nouveaux nanovecteurs dotés d’une très forte charge en principes actifs ont montré une excellente pénétration du biofilm ou du mucus trachéal humain et une excellente capacité à éradiquer les biofilms de Pseudomonas aeruginosa à une concentration environ 16 fois plus faible que la tobramycine seule. Cette étude, publiée dans Angewandte Chemie International Edition, illustre le potentiel des inhibiteurs du quorum sensing à diminuer la densité bactérienne des voies respiratoires et offrent des perspectives cliniques pour la récupération de la fonction pulmonaire. L’objectif ultime est d’améliorer la qualité de vie des patients atteints de troubles pulmonaires par infection à Pseudomonas aeruginosa. Légende Figure : Illustration du co-assemblage de la Tobramycine et d’une quinolone inhibitrice du quorum sensing au sein d’un vecteur d’hydrogénosulfate de squalényle et du mode d’action supposé de ces nanoparticules à tous les stades des infections respiratoires à Pseudomonas aeruginosa. Contact : patrick.couvreur@universite-paris-saclay.fr ou didier.desmaele@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
March 29, 2020 1:14 PM
|
Elias Fattal est Professeur de Pharmacotechnie à la Faculté de Pharmacie Châtenay-Malabry au sein de l’Université Paris-Saclay. Il a présidé l’Association de Pharmacie Galénique Industrielle (APGI) de 2003 à 2010 et a dirigé l'Institut Galien Paris-Saclay de 2010 à 2019
Elias Fattal est titulaire du diplôme d’état de Docteur en Pharmacie (1983), a obtenu le diplôme de Docteur de l’Université Paris-Sud en 1990 et a été pendant 2 années (1990- 1991) chercheur invité à l’Université de Californie, San Francisco aux USA.
Le professeur Fattal est l'auteur de plus de 260 articles à comité de lecture. Il a déposé 14 brevets internationaux et a reçu le Pharmaceutical Sciences World Congress Research Achievement (2007), the controlled Release Society fellow Award (2016).
Il a été récompensé en 2016 par l'Académie des sciences (Prix du Dr et de Mme Henri Labbé) et a reçu le prix Maurice-Marie Janot en 2018. Il est membre du comité de rédaction de 8 revues scientifiques.
Elias Fattal est également Président de la section 2 de l’Académie Nationale de Pharmacie depuis janvier 2020.

|
Scooped by
Life Sciences UPSaclay
February 18, 2020 4:34 AM
|
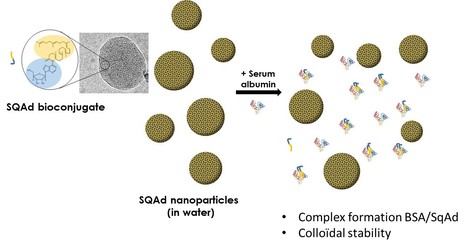
Une collaboration entre plusieurs équipes (CEA-Saclay (NIMBE et I2BC), Institut Galien Paris Sud, SOLEIL, LCE de l’Université de Bourgogne Franche-Comté et l’ILL) a permis de mettre en évidence le rôle particulier d’une protéine du plasma (la BSA, albumine du sérum bovin) dans le désassemblage de nanoparticules lipidiques utilisées comme vecteurs de principes actifs (famille des nanomédicaments). C’est sur une classe particulière de nanomédicaments que l’étude a été publiée dans Nanoscale. Des nanoparticules obtenues par auto-assemblage de squalène-adénosine (SQAd), un pro-médicament formé par le couplage entre un lipide, le squalène, et l’adénosine. Si l’efficacité de cette formulation a été démontrée (effets neuroprotecteurs démontrés chez le rat et la souris), il reste de nombreuses questions sur la stabilité, le mode d’action et l’interaction avec les protéines du sang de ces nanoparticules auto-assemblées après injection intraveineuse. En combinant différentes techniques de caractérisations structurales et spectroscopiques et en confrontant les résultats expérimentaux à des simulations, les chercheurs ont démontré l’existence d’une interaction entre les particules de SQAd et la BSA. Bien que la BSA ne semble pas former de couronne bien définie de protéines à la surface des nanoparticules, elle stabilise leur dispersion et surtout elle en extrait les molécules de SQAd pour former un complexe. Les nanoparticules de SQAd forment donc un réservoir de pro-médicaments dans la circulation du sang tandis que le complexe SQAd-BSA offre un deuxième niveau de transport et de délivrance du pro-médicament. Au-delà du cas particulier des nanoparticules de SQAd, ces études démontrent l’importance de la caractérisation des nanomédicaments en milieu complexe pour mieux comprendre leur évolution et optimiser leur action. Contacts : frederic.gobeaux@cea.fr ou fabienne.testard@cea.fr

|
Scooped by
Life Sciences UPSaclay
December 20, 2019 4:31 AM
|
L'Académie nationale de pharmacie dispose d'un nouveau bureau pour l'année 2020. Vice-président en 2019, Patrick Couvreur sera président pour cette nouvelle année. Il entend, dans un communiqué, "réhabiliter la chimie" dans l'enseignement des études de pharmacie. Il est également en faveur de la relocalisation de la production de médicaments pour prévenir les ruptures. Professeur émérite de pharmacotechnie (Institut Galien Paris-Sud, Faculté de Pharmacie de l'Université Paris-Saclay), membre de l’Institut Universitaire de France (IUF), Patrick Couvreur est reconnu au niveau international pour ses travaux pionniers dans le domaine de la vectorisation des médicaments (nanomédicaments) qui lui ont valu des distinctions scientifiques prestigieuses tant en France qu’à l’international : European Pharmaceutical Scientist Award de l’European Federation of Pharmaceutical Sciences (2011), Médaille de l’Innovation du CNRS (2012), l’European Inventor Award de l’Office Européen des Brevets (2013), le Speiser Award de l’ETH Zurich (2014), le T. & A. Higuchi Memorial Award de l’Académie Japonaise (2016), le Grand Prix Joseph Achille Le Bel de la SCF (2019). Il est membre de l’Académie des sciences, de l’Académie des technologies, de l’Académie nationale de médecine et de l’Académie nationale de pharmacie, membre étranger de la US National Academy of Medicine (E.-U.), de la US National Academy of Engineering, de l’Académie Royale de Médecine (Belgique) et de la Real Academia National de Farmacia (Espagne), docteur Honoris Causa de l’Université de Gand et de l’Université de Montréal (2020), et Chevalier de la Légion d’honneur. Auteur de plus de 550 publications, huit ouvrages, 91 brevets, il est le créateur de trois startups (Bioalliance, Medsqual et Squalpharma) dont l’une, cotée en bourse, occupe 60 employés. L’un des nanomédicaments qu’il a développés est arrivé en phase clinique III pour le traitement de l’hépatocarcinome résistant.

|
Scooped by
Life Sciences UPSaclay
November 6, 2019 10:48 AM
|
En conjuguant chimiquement la doxorubicine (Dox, un agent anticancéreux) au squalène (SQ, un lipide naturel), l’équipe du Prof Patrick Couvreur (Institut Galien Paris-Sud CNRS/UPSud, Châtenay-Malabry) a montré, dans un article publié dans la revue ACS Nano, qu’il était possible de construire des nano-objets de forme cylindrique. Des techniques de cryo microscopie électronique à transmission (cryo-TEM), de microscopie de force atomique (AFM), de diffraction RX aux petits angles et de balance de Langmuir ont été associées à de la modélisation moléculaire (UMR CNRS 6249, Université de Bourgogne Franche-Comté) pour comprendre la manière dont les bioconjugués de doxorubicine-squalène (SQ-Dox) s’associent pour former des édifices supramoléculaires de forme allongée (filomicelles ou nanotubes plus ou moins longs). La formation de ces nano-structures résulte, en effet, des propriétés physiques remarquables du bioconjugué de SQ-Dox qui mettent en jeu l'empilement (« stacking ») et les interactions électrostatiques de la doxorubicine avec les interactions hydrophobes du squalène. Les chercheurs ont, en outre, démontré qu’il était possible de manipuler la matière à l’échelle nanométrique puisque la forme, la taille, la flexibilité et les propriétés de surface de ces nanoparticules pouvaient être modulées en jouant sur la concentration du bioconjugué, la force ionique du milieu de suspension et la nature du contre-ion utilisé. Ces travaux montrent donc aussi que la structure supramoléculaire de nanoparticules dans le tube à essai et dans un milieu biologique riche en ions peuvent être très différentes. Ils permettent enfin de mieux comprendre les observations précédentes, concernant la résidence plasmatique prolongée de ces nanomédicaments après administration intraveineuse (publiées dans PNAS 2014). Contact : patrick.couvreur@u-psud.fr

|
Scooped by
Life Sciences UPSaclay
September 15, 2019 10:06 AM
|
Le Conseil d’administration de la Société Chimique de France (SCF) a décidé de décerner Le Grand Prix Joseph-Achille Le Bel 2019 au Professeur Patrick Couvreur. Patrick Couvreur est reconnu au niveau international pour ses travaux dans le domaine de la vectorisation des médicaments pour le traitement du cancer. Il dirige une équipe au sein de l'Institut Galien Paris-Sud (UMR UPSud/CNRS 8612) à la Faculté de Pharmacie de l'UPSud à Châtenay-Malabry. La communauté des chimistes représentée par la SCF tient ainsi à saluer sa contribution précieuse au rayonnement de la Chimie, tout particulièrement son rôle pionnier dans le domaine de la vectorisation des médicaments, son rôle capital dans le domaine des nano-médicaments et la levée des verrous de l’encapsulation physique, ainsi, enfin, que pour son invention du concept de « squalénisation ». Toutes nos félicitations !
|

|
Scooped by
Life Sciences UPSaclay
February 28, 2021 12:29 PM
|
Patrick Couvreur, membre de l’Académie des Sciences et chercheur à l’Institut Galien Paris-Saclay – IGPS (UMR 8612 CNRS/UPSaclay, Châtenay-Malabry) vient de publier avec Daniel Louvard (membre de l’Académie des Science, et chercheur à l’Institut Curie), une revue dans les Comptes Rendus Biologies de l’Académie des Sciences qui fait le point sur les différentes approches thérapeutiques qui ont été suivies pour traiter l’infection à SARS-CoV-2, ainsi que les troubles liés à l’inflammation paradoxale qui en découlent. Cet article est accompagné d’un second article dans la même revue par Alain Fischer sur les vaccins. Tous deux sont issus des travaux de la cellule de crise de l'Académie des Sciences. Contact : patrick.couvreur@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
February 6, 2021 9:50 AM
|
Portrait Jeune Chercheur - Thanh Duc Mai, Maitre de Conférences à la Faculté de Pharmacie
Thanh Duc MAI est Maitre de Conférences en chimie analytique à la Faculté de Pharmacie de l’UPSaclay, et effectue ses recherches à l’Institut Galien Paris-Saclay (IGPS, UMR 8612 CNRS/UPSaclay, Châtenay-Malabry) depuis septembre 2017. Ces dix dernières années, il a co-fondé et animé la plate-forme scientifique CE-Vietnam visant à promouvoir la recherche et mettre en place des collaborations dans le domaine de l’analyse miniaturisée entre l’IGPS et différentes universités et institutions au Vietnam. Entre 2015-2019, il a été co-fondateur et conseilleur scientifique de la StartUp EcyTech (Suisse), dont le but est de développer des instruments compacts et peu-couteux pour l'analyse de l'eau, le contrôle des aliments, le dépistage clinique et l'analyse des médicaments contrefaits. Après un doctorat en chimie analytique (conception et développement d’instrumentation) à l'Université de Bâle (Suisse) en 2011, il a poursuivi sa recherche post-doctorale dans différentes institutions en France. Ses activités de recherche actuelles à l’IGPS sont focalisées sur le développement de nouvelles approches (méthodologies et instruments) électrocinétiques pour la préconcentration et la séparation de biomolécules, de nanoparticules et de vésicules extracellulaires. Ses recherches visent à la détection sensible et sélective de biomarqueurs à base de protéines / peptides dans des matrices biologiques complexes. Il a conçu et mis en œuvre des designs instrumentaux innovants pour la chimie analytique, notamment le ‘DropLab’ (ANR JCJC, qui combine le traitement des échantillons en gouttes microfluidiques avec l’EC digitale), le ‘magneto-CE’ (CNRS Instrumentation aux limites, qui exploite la puissance de l’immuno-dosage sur les billes magnétiques avec l’EC) et le Lego-CE (instrument modulable inspiré par les jeux du Lego). Avec le support de l’université Paris-Saclay, il a récemment mis en place des actions visant à animer des projets de recherche collaboratifs impliquant l’utilisation de l’électrophorèse capillaire et la microfluidique au Vietnam, avec la participation de 5 sociétés françaises dans ces domaines depuis 2019. ‘Chemistry Is Like Cooking Just Don't Lick The Spoon’ - C’est pour cette raison que je fais de la recherche en chimie analytique avec joie. Contact : thanh-duc.mai@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
November 17, 2020 6:27 AM
|
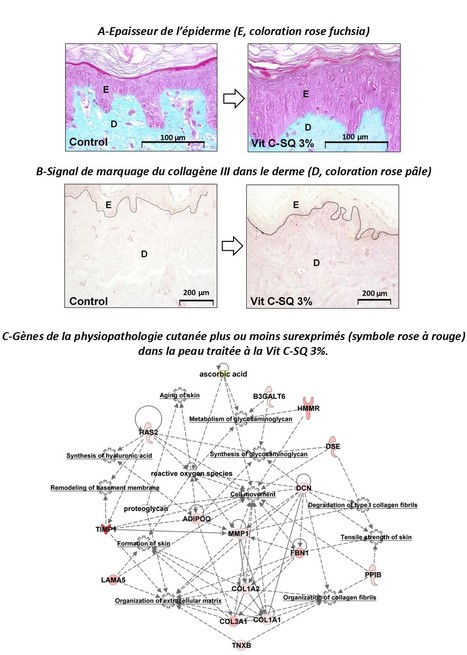
Il est bien connu que la vitamine C (Vit C) exerce, par son activité anti-oxydante, un effet bénéfique sur la peau et qu’elle stimule la production de collagène. Sachant que les collagènes de types I et III sont de moins en moins bien synthétisés avec l’âge, le développement de formulations capables de libérer la Vit C au niveau cutané présente un grand intérêt. Cependant, la Vit C ne franchit pas la barrière cutanée constituée par le stratum corneum et elle s’oxyde rapidement. Dans une étude parue dans Scientific Reports, les chercheurs de l’Institut des Sciences Moléculaires d’Orsay (ISMO UMR 8214 CNRS/UPSaclay, Orsay), de l’Institut Galien Paris-Saclay (IGPS UMR 8612 CNRS/UPSaclay, Châtenay-Malabry) et de l’UMS IPSIT (Châtenay-Malabry) ont proposé une stratégie qui consiste à coupler la Vit C au squalène (SQ), composé naturel lipophile présent naturellement au niveau de la peau, notamment dans le sébum. Les bioconjugués amphiphiles Vit C-SQ ont été appliqués sur des explants de peau humaine provenant de donneurs, dans le cadre d’une collaboration avec la société Bio-EC. Les explants ont été maintenus en survie pendant dix jours, permettant l’application régulière de produits (Vit C-SQ, Vit C libre et SQ seul ainsi que d’autres dérivés à base de Vit C comme témoins comparatifs). A la fin du traitement, des coupes histologiques, des microdissections et des analyses d’expression de gènes et de protéines ont été réalisées. Il a été découvert que le bioconjugué Vit C-SQ permettait un épaississement considérable de l’épiderme (Figure) comparativement à la Vit C libre ou par rapport à d’autres produits à base de Vit C. De plus, la production de collagène III a été améliorée par la Vit C-SQ dans une proportion significativement plus importante que tous les autres produits testés. Le bioconjugué a favorisé l’expression transcriptionnelle de gènes contribuant à la résistance à la traction et à la souplesse de la peau, ainsi que d’un gène codant pour un inhibiteur de collagénase. La Vit C-SQ a, en outre, amélioré la production des glycosaminoglycanes (GAGs) agissant comme réservoirs de facteurs de croissance, de même que l’expression de gènes impliqués dans la biosynthèse et l’activité de l’acide hyalyronique, facteur d’hydratation cutanée. Ces résultats positionnent les bioconjugués de Vit C-SQ comme un candidat de choix pour la formulation de crèmes anti-âge à usage cosmétique. Légende Figure : le bioconjugué Vit C-SQ permet un épaississement (+60%) de l’épiderme (A) et augmente (+100%) la biosynthèse du collagène III dans le derme (B) de même que l’expression transcriptionnelle d’un réseau de gènes impliqués dans la physiopathologie cutanée (C), après dix jours de traitement sur des explants de peau humaine. Contact : ruxandra.gref@universite-paris-saclay.fr ou claudine.delomenie@universite-paris-saclay.fr ou patrick.couvreur@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
October 25, 2020 5:52 PM
|
Patrick Couvreur, professeur émérite à l’Institut Galien Paris-Saclay (IGPS - Université Paris-Saclay, CNRS), est un pionnier du nanomédicament, une approche qui permet aux molécules thérapeutiques de cibler directement les tissus et les cellules des patients atteints de maladies graves (cancers, maladies du système nerveux). À la frontière entre la galénique, la chimie des matériaux, la pharmacologie et les nanotechnologies, les recherches de Patrick Couvreur ont de nombreuses fois été récompensées dans le monde entier, et ont débouché sur la création de plusieurs start-up innovantes. Le chercheur est également membre des académies scientifiques de plusieurs pays en Europe et aux États-Unis. En France, il est devenu président de l’Académie nationale de pharmacie en 2020. Lice la suite ICI.

|
Scooped by
Life Sciences UPSaclay
September 1, 2020 5:03 PM
|
L'inflammation, caractéristique commune de nombreuses maladies, est un mécanisme immunitaire de défense face aux agressions tels que des agents infectieux, des lésions physiques ou un stress métabolique. Elle a pour objectif de reconnaître et d’éliminer toutes substances étrangères afin d’assurer la survie et le maintien de l’homéostase des tissus. Cependant, sous certaines conditions, la réponse inflammatoire peut devenir incontrôlée et conduire à des états pathologiques. Les stratégies thérapeutiques actuelles visent surtout à atténuer les symptômes principalement via l’utilisation de médicaments anti-inflammatoires stéroïdiens ou non-stéroïdiens. Mais ces traitements sont limités par une bio-distribution souvent non-spécifique, une faible biodisponibilité ou encore un temps de demi-vie plasmatique trop court, conduisant à des effets secondaires indésirables. L’utilisation de nanomédicaments – i.e. des nanoparticules chargées avec un principe actif – pour cibler l’inflammation pourrait permettre de surmonter ces inconvénients. En effet, l’obtention de nanomédicaments avec des tailles, morphologies et potentiels électriques de surface facilement modulables offre une solution prometteuse pour le traitement des maladies inflammatoires. Cela peut se faire par l’exploitation d’un système vasculaire fragilisé et plus perméable au niveau de la zone inflammatoire, ou par le ciblage actif de marqueurs sur-exprimés par les cellules inflammatoires et immunitaires. Dans une revue publiée dans le journal Advanced Drug Delivery Reviews, après avoir présenté un bref aperçu de la physiopathologie de l’inflammation et des stratégies thérapeutiques actuelles, les auteurs (R. Brusini, M. Varna et P. Couvreur, Institut Galien Paris-Saclay UMR 8612 CNRS/UPSaclay, Faculté de Pharmacie, Châtenay-Malabry) discutent des avantages et inconvénients des nanomédicaments développés ces 5 dernières années pour la résolution des troubles inflammatoires. L’article décrit également les nano-vecteurs en essai clinique ou déjà sur le marché. Contact : patrick.couvreur@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
June 11, 2020 6:01 AM
|
La polydopamine (PDA) est un polymère bioinspiré du processus d’adhésion des moules sur les rochers. La PDA présente des propriétés très intéressantes pour la conception des nanovecteurs à propriétés multifonctionnelles. En effet, il s’agit d’un polymère possédant des propriétés photothermiques intéressantes, il est facilement fonctionnalisable, biocompatible et biodégradable du fait de sa similarité structurale avec un biopolymère, qui est la mélanine (eumélanine). Afin de concevoir un nanomédicament à base de PDA et à propriétés multifonctionnelles, l’équipe de Physico-Chimie des Surfaces de l'Institut Galien (UMR 8612 CNRS/UPSaclay/LabEx LERMIT, Faculté de Pharmacie, Châtenay-Malabry) a récemment établi des conditions expérimentales étroitement contrôlées qui permettent de Pegyler et de moduler la taille, le rendement et les propriétés mécaniques des nanoparticules de PDA. En outre, les propriétés nanomécaniques des nanoparticules de PDA présentant différentes tailles, ont été aussi étudiées par nano-indentation AFM (Microscope à Force Atomique). Les résultats, publiés dans Journal of Materials Chemistry B ont démontré pour la première fois que l'élasticité des nanoparticules de PDA diminue avec leur taille. Ces caractéristiques ont été reliées à l'ordre géométrique plus élevé des fractions oligomériques de PDA au sein des nanoparticules de plus grande taille. Ces propriétés mécaniques modulables pourraient ainsi contrôler l’internalisation cellulaire des nanoparticules de PDA, leur pénétration dans les tissus ainsi que leur biodistribution. Contact : ali.makky@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
May 3, 2020 11:47 AM
|
Une équipe de l’Institut Galien (CNRS/UPSaclay, Faculté de Pharmacie, Châtenay-Malabry) vient de mettre au point des nanoparticules efficaces dans le traitement des processus inflammatoires sévères que l’on retrouve dans de nombreuses pathologies et notamment dans des infections dues au covid-19. Ces travaux sont publiés dans la revue Science Advances lundi 27 avril 2020. Les processus inflammatoires incontrôlés posent un problème de santé majeur car ils sont à l'origine de nombreuses pathologies qui peuvent être sévères voire létales. Ainsi, certains patients atteints par le virus Covid-19 voient leur état se détériorer après une réaction inflammatoire incontrôlée qui provoque une insuffisance respiratoire, nécessitant parfois intubation et réanimation voire entrainant le décès. Actuellement très peu de traitements s’avèrent efficaces pour traiter ces inflammations sévères et ceux qui existent ont des effets secondaires indésirables. Les études menées depuis près de deux décennies tendent à montrer que ces états d’inflammation aiguë seraient provoqués par la conjonction de deux facteurs : une inflammation combinée à un épisode de stress oxydant (phénomène d’oxydation chimique subi par l’organisme), contribuant à s'alimenter mutuellement et établissant ainsi un cercle vicieux capable de perpétuer et de propager la réponse inflammatoire A l’Institut Galien, des équipes de recherche sont spécialisées dans l’élaboration de nanomédicaments. L’introduction des nanotechnologies en pharmacologie a révolutionné l’administration des médicaments, notamment grâce au principe de vectorisation. La vectorisation d’un médicament est basée sur le principe d’adressage, qui consiste à encapsuler le médicament dans un nanovecteur (le plus souvent un liposome, ou une nanoparticule). Généralement comprise entre 20 et 300 nanomètres, la petite taille de ces dispositifs thérapeutiques leur permet de protéger le principe actif, de traverser certaines barrières biologiques et de délivrer le médicament plus efficacement dans l’organisme. L’objectif de l’adressage est donc d’améliorer l’efficacité des traitements tout en obtenant une meilleure maîtrise de leur index thérapeutique, ce qui permet de réduire leur toxicité et d’en limiter les effets secondaires. En collaboration avec la Plateforme d’Histologie Immunopathologie de Clamart (PHIC) de l’Institut Paris Saclay d'innovation thérapeutique (INSERM/CNRS/UPSaclay), les chercheurs de l’Institut Galien, ont combiné différents principes actifs au sein d’une même nanoparticule en conjuguant le squalène, un lipide naturel, avec l'adénosine, un immunomodulateur, puis en y associant l’alpha-tocophérol, un antioxydant naturel. Leur étude in vivo sur un modèle animal présentant un choc septique a démontré qu’en exploitant les dysfonctionnements de la barrière endothéliale au niveau des sites de l'inflammation aiguë, ces nanoparticules multi-médicaments pouvaient délivrer les agents thérapeutiques de manière ciblée et améliorer ainsi les chances de survie de manière significative. Ces résultats prometteurs pourraient désormais être complétés par des études cliniques pour espérer à terme parvenir au développement d’un nouveau médicament efficace pour lutter contre les inflammations sévères et incontrôlées et ouvrir de nouvelles pistes pour lutter contre les réactions inflammatoires paradoxales telles que celle associée à l’infection par covid-19. Contact : patrick.couvreur@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
March 31, 2020 11:04 AM
|
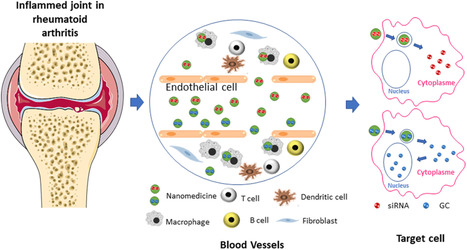
La nanomédecine permet d’améliorer les traitements de nombreuses maladies en adressant sélectivement la substance active vers sa cible, tout en diminuant ses effets secondaires. L’article de revue publié récemment par l’équipe d’Elias Fattal (Institut Galien Paris-Sud-UMR CNRS 8612 Faculté de Pharmacie de UPSaclay, Châtenay-Malabry) dans Wiley Interdiscip Rev Nanomed Nanobiotechnol aborde ces questions dans le cadre des innovations pharmaceutiques dans le traitement de l’arthrite rhumatoïde. En effet, la biodistribution préférentielle des nanomédicaments au niveau des sites inflammatoires permet à des substances actives telles que les glucocorticoïdes d'être plus efficaces à des doses plus faibles, des fréquences d'administration plus espacées et surtout, d'induire beaucoup moins d'effets secondaires. Plus récemment, les acides nucléiques tels que les ARN interférents (siARN), les microARn (miARN) ou les anti-miARN (dénommés aussi antagomir) ont fait la preuve de leurs potentialités pour réprimer certains gènes ou voies de signalisation impliquées dans l’arthrite rhumatoïde. L’article de revue démontre comment ces acides nucléiques administrés via des nanomédicaments voient leur pénétration au sein des cellules inflammatoires augmenter avec une meilleure distribution subcellulaire. Les nanomédicamens protègent enfin ces molécules fragiles contre la dégradation enzymatique. Ceci apparait clairement dans le cas des siARN qui, en réprimant les gènes de certaines cytokines permettent d’obtenir des rémissions importantes de la pathologie dans des modèles de souris ou de rat. Enfin, en se basant sur certains exemples issus de la littérature, il est démontré qu’une combinaison de plusieurs substances actives peut être réalisée au sein du même nanomédicament permettant ainsi d’augmenter l’efficacité du traitement en agissant de manière concomitante sur des cibles différentes. Contact : elias.fattal@universite-paris-saclay.fr

|
Scooped by
Life Sciences UPSaclay
March 13, 2020 1:12 PM
|
Des chercheurs de l'Institut Galien Paris-Sud (CNRS/Université Paris-Saclay, Faculté de Pharmacie, Châtenay-Malabry) ont mis au point une stratégie de synthèse de médicaments anticancéreux à injecter par voie sous-cutanée. La start-up Imescia créée en juin 2019 développe ces nouveaux traitements dont le mode d'administration permettra d'utiliser des anticancéreux plus efficaces, aujourd'hui inutilisables en raison de leur toxicité locale.
illustration
Les traitements anticancéreux sont pour la plupart administrés par voie intraveineuse, à l'hôpital. L'injection sous-cutanée permettrait de simplifier le traitement. Mais cette voie est aujourd'hui limitée par la toxicité locale des molécules anticancéreuses. Pour s'affranchir de cet obstacle, des chercheurs de l'Institut Galien Paris-Sud1 ont mis au point une stratégie de synthèse simple et transposable à plus grande échelle de prodrogues polymères anticancéreuses sans toxicité.
Elle consiste à coupler une molécule anticancéreuse avec un agent de contrôle de polymérisation radicalaire, qui va ensuite amorcer la polymérisation d'un monomère. Le résultat est une prodrogue constituée d'une molécule de principe actif, liée à l'extrémité d'une courte chaîne de polymère, qui est libérée après injection de manière contrôlée et prolongée dans le sang. Au-delà de la simplicité de l’administration, cette approche innovante permet d’améliorer l’efficacité des traitements. La start-up Imescia a été fondée en juin 2019 pour développer ces nouveaux traitements brevetés.
Cette technologie peut s'adapter à de nombreuses molécules anticancéreuses, avec différents polymères. « Nous nous focalisons sur des molécules anticancéreuses hautement efficaces, mais qui n'ont pas pu être utilisées en raison notamment de leur toxicité », indique Tanguy Boissenot, PDG et confondateur d'Imescia4. La start-up développe son propre produit, un traitement anticancéreux par voie sous-cutanée qui est au stade des études précliniques. En parallèle, des partenariats sont en cours de négociation avec des laboratoires pharmaceutiques pour mettre au point des traitements basés sur des molécules actives qui jusqu'ici n'ont pas pu déboucher sur des traitements. Pour financer ces activités, une première levée de fonds devrait être finalisée au milieu de l'année 2020. Contact : tanguy.boissenot@imescia.com

|
Scooped by
Life Sciences UPSaclay
December 20, 2019 4:26 PM
|
Dans le cadre d’un projet soutenu par le labex LERMIT, les équipes d’Elias FATTAL (Institut Galien Paris-Sud, UMR 8612 CNRS/UPSud, Faculté de Pharmacie UPSud, Châtenay-Malabry) et d’Eric DORIS (Service de Chimie Bioorganique et de Marquage, CEA-Joliot, Saclay) ont mené une étude comparative approfondie sur la nanotoxicité de vecteurs micellaires constitués d’acide pentacosadiynoique couplé au polyéthylène glycol. Ces vecteurs ont été évalués sur une lignée de macrophages RAW 264.7, soit sous leur forme non-polymérisée (dynamique par nature), soit polymérisée qui correspond à une forme stabilisée de la micelle. Alors que les constituants des micelles non polymérisées s’accumulent dans les bicouches lipidiques de la membrane plasmique, les micelles polymérisées pénètrent dans les cellules selon un mécanisme d’endocytose. En raison d’une distribution intracellulaire très différente, les micelles polymérisées induisent une plus faible cytotoxicité, pas d’apoptose, aucune réponse inflammatoire et aucune génotoxicité. Ces résultats, publiés dans la revue Nanoscale, montrent que de simples transformations dans l’architecture d’un nanomédicament entrainent des modifications importantes du trafic intracellulaire et de la toxicité qui peut en résulter. Contact : elias.fattal@u-psud.fr ou eric.doris@cea.fr

|
Scooped by
Life Sciences UPSaclay
December 13, 2019 12:57 PM
|
Une nouvelle structure d’agrégats d’alpha-synucléine a été résolue à l’échelle atomique, par cryo-microscopie électronique. Ces travaux menés par une équipe du Laboratoire des Maladies Neurodégénératives (CEA-Jacob, MIRCen, Fontenay-aux-Rose), en collaboration avec l'Institut Galien Paris Sud (IGPS, Châtenay-Malabry)ont fait l’objet d’une publication dans la revue eLife. La résolution de cette structure ouvre de nouvelles perspectives pour le développement de ligands ciblant spécifiquement ces agrégats dans la maladie de Parkinson. Lire la suite ICI.

|
Scooped by
Life Sciences UPSaclay
October 10, 2019 5:36 AM
|
Elias Fattal a été élu Président de la section 2 de l'Académie Nationale de Pharmacie.
A partir de janvier 2020, le Professeur Elias Fattal, directeur de l'Institut Galien UMR-8612 de la Faculté de Pharmacie de l'Université Paris-Sud, succèdera à Christine Capdeville-Atkinson à la présidence de la section 2 de l'Académie Nationale de Pharmacie. Cette section intitulée Sciences pharmaceutiques appliquées au médicament et aux autres produits de santé, est dédiée à l'étude des sujets relatifs à la connaissance du médicament et des produits de santé. En particulier dans les domaines de la pharmacie galénique, la pharmacologie expérimentale et clinique, la toxicologie expérimentale, la clinique ainsi que la botanique, la pharmacognosie et la cosmétologie. Elias Fattal succèdera à Christine Capdeville-Atkinson et prendra ses nouvelles fonctions à partir de Janvier 2020.
|



 Your new post is loading...
Your new post is loading...