Bulletin d'information scientifique de l'IHU - Nous avons le droit d'être intelligents !
Pr Didier Raoult, Directeur de l'IHU Méditerranée Infection
La lutte contre l’épidémie de COVID-19 a impliqué l’exploration de nombreuses pistes thérapeutiques, qui ont donné lieu à des recherches in vitro et in vivo. Cependant, les praticiens dans le monde n’ont pas attendu les résultats de ces recherches pour utiliser ce qui leur paraissait être le traitement le plus adéquat (1). Cela oblige à faire preuve de rapidité dans la réalisation de recherches puis dans la diffusion des résultats aux médecins confrontés à l’épidémie sur le terrain, pour orienter leur prise en charge thérapeutique des patients.
L’utilisation de traitements potentiels sur des patients permet de produire des données, utilisables ensuite dans la recherche. Dans la communauté scientifique, la réalisation d’essais cliniques randomisés en double-aveugle est devenue le gold standard permettant de valider l’efficacité d’un traitement. Cependant, lorsque l’urgence est de soigner des patients dont la vie est en danger, il n’est pas éthique de leur donner un placebo lorsque l’état de l’art donne au médecin l’intime conviction que la balance bénéfice-risque est en faveur de l’administration du traitement qu’il souhaite expérimenter. Nous ne devons donc pas oublier que des études simple-bras, sans randomisation, peuvent être tout aussi probantes que des études randomisées.
Deux éléments nous apparaissent cruciaux pour qu’une étude réalisée sans randomisation soit significative. Il faut d’abord qu’elle étudie des end-point clairement identifiés. Pour le COVID19, nous en identifions trois : la mortalité, le passage en réanimation, et la charge virale. Il faut en outre qu’elle soit comparative. Il faut que l’étude compare les résultats suite à l’utilisation d’un traitement à des séries de résultats historiques, ou à une série de résultats dans d’autres centres de soin.
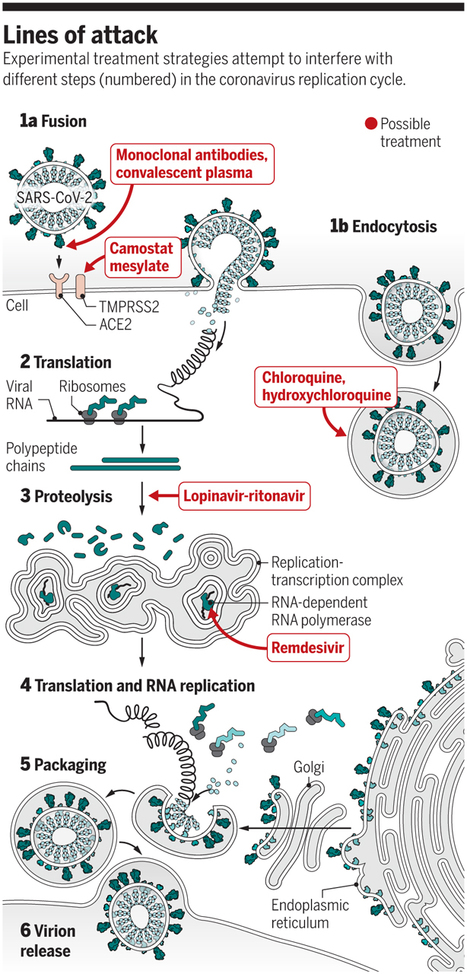
Aujourd’hui, 5 pistes thérapeutiques se dégagent pour lutter contre l’épidémie de coronavirus et sont l’objet d’essais cliniques dans le monde : la chloroquine/hydroxychloroquine, l’hydroxychloroquine combinée à l’azithromycine, le lopinavir/ritonavir (Kaletra), le remdesivir et l’utilisation de plasma de patients guéris d’une infection à COVID-19. Nous nous proposons de passer en revue les résultats publiés au sujet de ces 5 pistes thérapetiques.
- Des résultats in vitro ont montré une efficacité de la chloroquine et de l’hydroxychloroquine (3). Sur la base de ce travail, les résultats de trois études ont été publiées : une en France portant sur 24 patients et concluant à l’efficacité de ce traitement (4), et deux en Chine, la première ne concluant pas à une efficacité suite à l’expérimentation sur 15 patients avec groupe contrôle (3), la deuxième ayant conclu à l’efficacité de l’hydroxychloroquine suite à une expérimentation sur 31 patients avec groupe contrôle (5). Deux limites dans ces études limitent aujourd’hui la connaissance. D’abord, ces études ne rapportent ni la même durée de traitement, ni la même posologie. Ensuite, les deux études chinoises ne donnent pas de précisions concernant les autres traitements utilisés dans le cadre du protocole.
- Concernant l’utilisation de la combinaison hydroxychloroquine + azithromycine, notre équipe a publié deux études observationnelles, le premier portant sur 80 patients (6), le deuxième portant sur 1061 patients (7). Tous deux concluent à une efficacité de ce traitement pour les trois end-points définis plus haut. Nos points de comparaison sont, concernant la durée de portage viral, des études chinoises sur l’histoire naturelle de la maladie (8), et concernant les aspects cliniques, les études réaliséesdans des services n’utilisant pas cette prescription.
- Concernant le kaletra, une étude comparative avec deux bras a conclu à son inefficacité (9). Son efficacité in vitro reste à démontrer.
- Concernant le remdesivir, une étude intéressante financée par Gilead a été publiée dans le New England Journal of Medicine (10). Elle permet uniquement de conclure à la toxicité du remdesivir pour les patients à qui il a été administré (60% d’effets secondaires, 23% d’effets secondaires graves, 8% menant à l’arrêt du traitement). S’il est encourageant de constater que des équipes sérieuses, comme celle qui a écrit cet article, comprennent qu’il n’est pas éthique de donner un placebo à un patient dont la vie est en danger, il ne faut pas que cela implique d’oublier qu’une étude qui ne comporte ni end-point, ni comparatif, ne peut permettre de conclure quoi que ce soit.
- L’utilisation de plasma est une idée théoriquement intéressante. Deux études ont été publiées à ce jour (11,12). Scientifiquement, cette solution pose problème car l’utilisation du plasma est difficile à envisager dans les formes non-graves de la maladie. Dans les formes graves, le problème n’est pas virologique mais immunitaire.
Au vu de ces données de la littérature, les équipes médicales de l’IHU, comme médecins s’étant engagés à respecter le serment d’Hippocrate, ont pris la décision de poursuivre le traitement des patients atteints de COVID19 avec le protocole hydroxychloroquine+azithromycine, en l’attente de nouveaux résultats.
Yanis Roussel, Didier Raoult



 Your new post is loading...
Your new post is loading...