Modulation of insect immunity to control vector-borne diseases
By Dr. Chinta Sidharthan
Dec 19 2022
Reviewed by Aimee Molineux
-------
NDÉ
Traduction
Contexte
La dengue, le paludisme, la filariose et le Zika sont quelques-unes des principales maladies infectieuses transmises par des insectes dans le monde. Au cours des dernières décennies, la dengue et le paludisme ont augmenté de manière significative. En outre, bien que les insecticides réduisent la propagation des maladies transmises par les insectes dans certaines régions du monde, la résistance croissante aux insecticides dans les populations naturelles d'insectes indique la nécessité de trouver d'autres stratégies pour limiter la transmission des maladies transmises par les insectes.
L'un des domaines qui retient l'attention est l'amorçage immunitaire pour réduire la transmission de la maladie. La compétence du vecteur, c'est-à-dire sa capacité à transmettre l'agent pathogène, dépend de sa réponse immunitaire. Chez les insectes, l'immunité est régulée par des voies de signalisation telles que les voies c-Jun N-terminal kinase (JNK), Janus kinase-signal transducteur et activateur de transcription (JAK-STAT), immunodéficience (IMD), Toll et interférence de l'acide ribonucléique (ARNi). Les recherches récentes sur les maladies à transmission vectorielle ont porté sur l'utilisation de ces mécanismes moléculaires pour cibler l'amorçage immunitaire et réduire la transmission des maladies.
Le système immunitaire des insectes
Comme les insectes dépendent d'un système immunitaire inné, on pensait qu'ils n'avaient pas la capacité de développer et de maintenir une réponse immunitaire adaptative après une exposition à des agents pathogènes. Cependant, des études ont mis en évidence l'existence d'un amorçage immunitaire chez les insectes, où l'exposition à des agents pathogènes entraîne une modification durable des cellules qui renforce la réponse immunitaire lors d'infections ultérieures.
Chez les blattes (Periplaneta americana), il a été démontré que l'immunisation par Pseudomonas aeruginosa inactivé protégeait les insectes contre les infections par la bactérie vivante, et que les effets duraient des semaines. Des résultats similaires ont été observés chez la drosophile immunisée avec Streptococcus pneumoniae. Les études montrent que l'amorçage immunitaire peut être spécifique ou non de l'agent pathogène et peut s'étendre à d'autres stades de vie de l'insecte. Lorsque P. americana immunisé contre P. aeruginosa a été exposé à d'autres bactéries, les effets protecteurs n'ont duré que trois jours. Cependant, il a été démontré que l'amorçage chez les larves d'insectes augmentait l'immunité chez la forme adulte.
Il a également été démontré que d'autres facteurs, tels que le stress dû à un manque de nutrition, la compétition et les blessures, produisent des phénotypes similaires à l'amorçage. Bien que les preuves suggèrent que l'amorçage immunitaire est similaire à la mémoire immunitaire, les voies et les mécanismes moléculaires restent largement inexplorés.
Preuve de l'amorçage immunitaire
L'immunité antivirale chez la drosophile adulte est renforcée lorsque les hémocytes produisent un petit ARN interférent (ARNi) viral secondaire en utilisant l'acide désoxyribonucléique (ADN) viral comme matrice. L'ARNi est délivré par des vésicules de type exosome à d'autres tissus de l'insecte. Une étude sur le virus C de la drosophile a montré que l'infection orale du virus chez les larves de drosophiles augmentait la tolérance à l'infection chez les formes adultes.
Les drosophiles femelles exposées à des virus à ARN simple brin positifs ont présenté un amorçage immunitaire transgénérationnel (TGIP) avec une immunité antivirale spécifique de la séquence et dépendante de l'ARN chez la progéniture pour les cinq générations suivantes. Des TGIP similaires ont été observés chez les larves de moustiques Aedes aegypti lorsque les femelles adultes ont été exposées au virus du chikungunya. Bien que l'on pense que l'ADN viral joue un rôle important dans la TGIP, les mécanismes de transfert et d'amplification de l'ADN viral restent flous.
Les moustiques anophèles ont montré une immunité renforcée dépendante des hémocytes contre les infections ultérieures après une exposition au Plasmodium. Des études ont signalé le rôle du microbiote intestinal dans l'établissement et le rappel de la mémoire immunitaire antiplasmodiale, qui est permanente et dépend des granulocytes circulants. Les lipides eicosanoïdes tels que les lipoxines et les prostaglandines jouent le rôle de molécules de signalisation dans l'immunité coordonnée observée dans divers tissus d'insectes.
Les hèmes-peroxydases HPX7 et HPX8, induites pendant l'infection par Plasmodium, médient la synthèse de la prostaglandine E2 (PGE2) par le microbiote de l'intestin moyen. La libération de PGE2 déclenche la libération du facteur de différenciation des hémocytes, qui est un complexe lipoxine-lipocaline. La PGE2 provoque également une augmentation de la double peroxydase par les cellules de l'adipocyte appelées oenocytes.
Une immunité entraînée
Des recherches récentes ont porté sur l'entraînement immunitaire, dans lequel les niveaux de transcription des effecteurs immunitaires reviennent à l'état basal après l'exposition initiale à l'agent pathogène. L'infection ultérieure entraîne une meilleure réponse des cellules effectrices que dans le cas de l'amorçage immunitaire. L'entraînement immunitaire (...)
L'étude
Can immune memory impact vector-borne disease transmission?
Despite its remarkable plasticity, activation of vector immunity often restricts infection under tolerable levels, instead of completely eliminating the pathogen [52]. Nevertheless, refractory or quasi-refractory populations are observed worldwide [53], and experimental infections of field-caught mosquitoes reveal remarkable variability between individuals. While stochastic variations [54] and genetic components [55,56] are important factors driving this heterogeneity, differences in individual life histories also shape host immunological status [57–60].
Immune priming, immune tolerance, and immune training are likely to be important modulators of individual vector competence. Recently, features of trained immunity were described in nonimmune vertebrate cells, such as epithelial and mesenchymal cells [61], and the role of the gut microbiota has been proposed [62]. Interestingly, the vector gut microbiota is also a major driver of mosquito immunity [63]. It remains to be established whether insect immune priming and trained immunity share some regulatory signaling pathways, such as those activated by the gut microbiota.
Thus, priming the immune system of insect vectors is a potential strategy to reduce disease transmission. Manipulation of larvae would be an interesting strategy to reduce vectorial capacity, as infection or immune challenge of larvae, nutritional manipulation, and intraspecific competition have been shown to enhance immunity in adult stages [26,27,64] and logistics to target larval breeding sites are well established [65–67]. While the epigenetic regulation of immunometabolism is an important factor driving susceptibility in vertebrates (and a target for therapeutics), it has only recently started to be investigated in models of disease vectors [40,68,69]. Further identification of molecular markers will make it possible to establish the frequency and intensity of such events in natural populations.
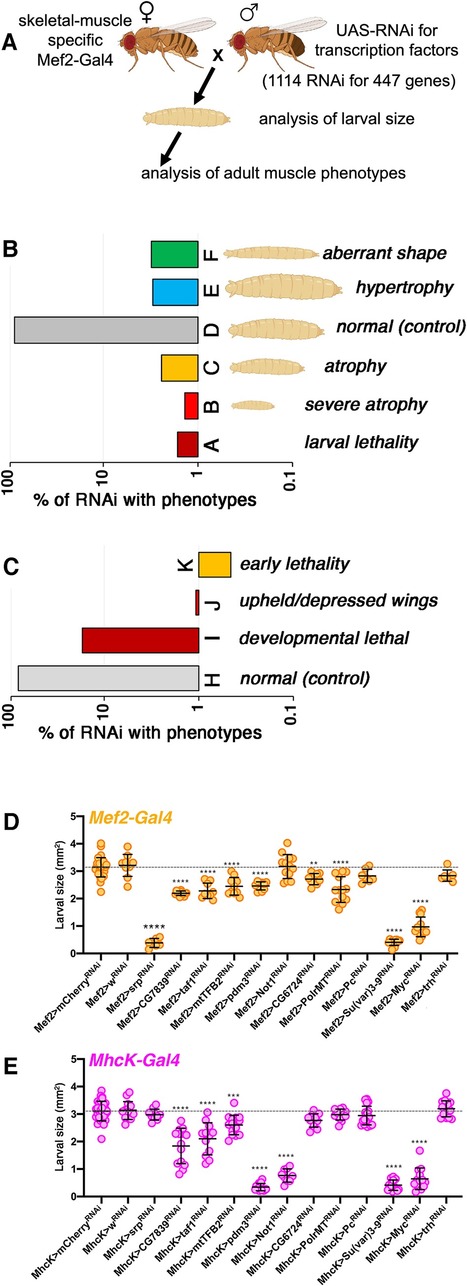
[Image] Immune priming in An. gambiae mosquitoes.



 Your new post is loading...
Your new post is loading...






https://www.scoop.it/topic/entomonews/?&tag=ARNi+%28ARN+interf%C3%A9rent%29